Сколько добавлять соли в раствор при минусовой температуре: Для чего добавляют соль в бетон и цементный раствор, сколько её нужно? | Строительный журнал САМаСТРОЙКА
- Для чего добавляют соль в бетон и цементный раствор, сколько её нужно? | Строительный журнал САМаСТРОЙКА
- Цементно-песчаный раствор. Цена на цементный раствор в СПб
- Эксплуатация, зарядка, хранение аккумуляторной батареи
- Содержание
- 1.
- 2. Основные характеристики аккумуляторных батарей
- 3.
- 4. Маркировка АКБ
- 5. Выбор и покупка АКБ
- 6. Установка АКБ
- 7. Рекомендации по эксплуатации и обслуживанию
- 8. Особенности эксплуатации АКБ в зимний период
- 9. Особенности эксплуатации АКБ в летний перио
- 10. Вопросы безопасности
- 11. Хранение аккумуляторной батареи
- 12. Приложения
- Добавление соли в лед в холодильнике
- Как сделать соляной раствор для дорог — Библиотека соли
- Соль и лед
- Как действует соль и обзор химикатов против обледенения
- Как холодно слишком холодно, чтобы мыть машину
- Фермерские стада будут счастливы, пока вода в корыте говорит жидкость
Для чего добавляют соль в бетон и цементный раствор, сколько её нужно? | Строительный журнал САМаСТРОЙКА
Соль в бетон и раствор: зачем и сколько?
Соль в бетон и раствор: зачем и сколько?
Содержание статьи:
- 1. Зачем добавляют соль в бетон
- 1.1. Сколько нужно добавлять соли в бетон и цементный раствор
Изменить свойства цементного раствора и бетона в лучшую сторону можно разными способами. Очень часто строители добавляют соль в бетон и раствор, которая является эффективной противоморозной добавкой. Соль позволяет работать со строительной смесью при отрицательных температурах воздуха и способна изменить в лучшую сторону её характеристики.
Конечно же, можно использовать специальные добавки на полимерной основе, которые не дадут замерзнуть воде на морозе, которая находится в растворе. Но все это существенно удорожает смесь. Ранее в строительном журнале samastroyka. ru уже рассказывалось про «народные» добавки в бетон и раствор. Упоминалось там и использование соли, но только совсем уж поверхностно. В данной статье будет рассказано, для чего добавляются соль в цементный раствор или бетон, а также её конкретные пропорции использования.
ru уже рассказывалось про «народные» добавки в бетон и раствор. Упоминалось там и использование соли, но только совсем уж поверхностно. В данной статье будет рассказано, для чего добавляются соль в цементный раствор или бетон, а также её конкретные пропорции использования.
Зачем добавляют соль в бетон
Добавление соли в бетон и цементный раствор даёт возможность вести строительные работы при отрицательных температурах окружающей среды. На застывание цементного раствора нужно примерно несколько дней, а вот при морозе, данный срок существенно сокращается. Из-за этого происходит разрушение строительной смеси изнутри, она становится рыхлой и непрочной.
Соль же добавленная в цементный раствор, не даёт воде замерзнуть некоторое время на морозе, что положительным образом сказывается на качестве раствора. Однако мнения строителей по поводу добавления соли в бетон и растворы на основе цемента, серьезно разделились.
Одни из них считают, что при добавлении соли в бетон, коррозия металлических элементов армирования резко возрастает. Другие же строители, наоборот, добавляют соль в раствор и считают такую добавку самой дешевой из всех противоморозных добавок. Соль позволяет применять растворы на основе цемента при отрицательной температуре воздуха.
Как бы там ни было, каждую добавку в бетон и цементный раствор нужно использовать на свой страх и риск. При этом обязательно следует знать правильные её пропорции по отношению к объему строительной смеси. В противном случае можно сделать только хуже.
Сколько нужно добавлять соли в бетон и цементный раствор
Количество соли в цементный раствор или бетон, всецело зависит от температуры окружающей среды. Добавляют соль в бетон и цементные растворы, только в том случае, если с ними приходится работать при отрицательных температурах, когда требуется не допустить быстрого замерзания воды и их разрушения вследствие этого.
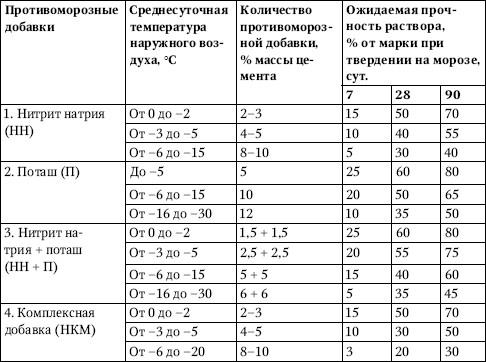
Так, например, при температуре воздуха от 0 до — 5 градусов, процентное содержание соли от общей массы строительной смеси, должно составлять примерно 2%. При температуре от -5 до -15 градусов, соль добавляют в цементный раствор не менее 4% от общей его массы.
Кроме того, учитывая высокие коррозионные процессы при добавлении соли в бетон, можно выделить один главный нюанс: использовать соль в качестве противоморозной добавки можно только для тех конструкций из бетона, в которых отсутствуют металлические элементы армирования. Например, при заливке бетоном отмостки, там, где не применяется армировка. При таком подходе, соль, в качестве противоморозной добавки, окажется самым дешевым вариантом.
Однако, по мнению все тех же самых экспертов, от использования бетона и цементных растворов при отрицательных температурах, лучше и вовсе отказаться. Желательно спланировать бетонные работы, таким образом, чтобы они не приходились на зиму. В любом случае, и прочность, и долговечность эксплуатации строительных конструкций с использованием бетона и цементных смесей, построенных в это время, будет намного ниже.
В любом случае, и прочность, и долговечность эксплуатации строительных конструкций с использованием бетона и цементных смесей, построенных в это время, будет намного ниже.
Читайте также:
Цементно-песчаный раствор. Цена на цементный раствор в СПб
Цементно-песчаный раствор
Цемент – главная составляющая подавляющего большинства строительных растворов. Он обладает прочностью и пластичностью, что и оказало влияние на его популярность. Цементный раствор незаменим при сооружении стен из кирпича, при работах по оштукатуриванию помещений и фасадов, при заливке полов и производстве бетона.
Для приготовления данного монтажного раствора используется мелкий щебень или песок. Нередко добавляются специальные вещества, обладающие особыми свойствами. При подготовке раствора очень важно соблюдать пропорции, чтобы предотвратить разрушение конструкций.
Цена за куб на монтажный раствор.
| Марка раствора | Пк3 | Пк4 |
| Раствор м75 | 2400 | |
| Раствор м100 | 2500 | |
| Раствор м150 | 2750 | 2800 |
| Раствор м200 | 2850 | 2900 |
| Раствор м250 | 2900 | 2950 |
| Раствор м300 | 3200 | 3250 |
Приготовление правильного цементно-песчаного раствора
В чистом виде цемент почти никогда не используется.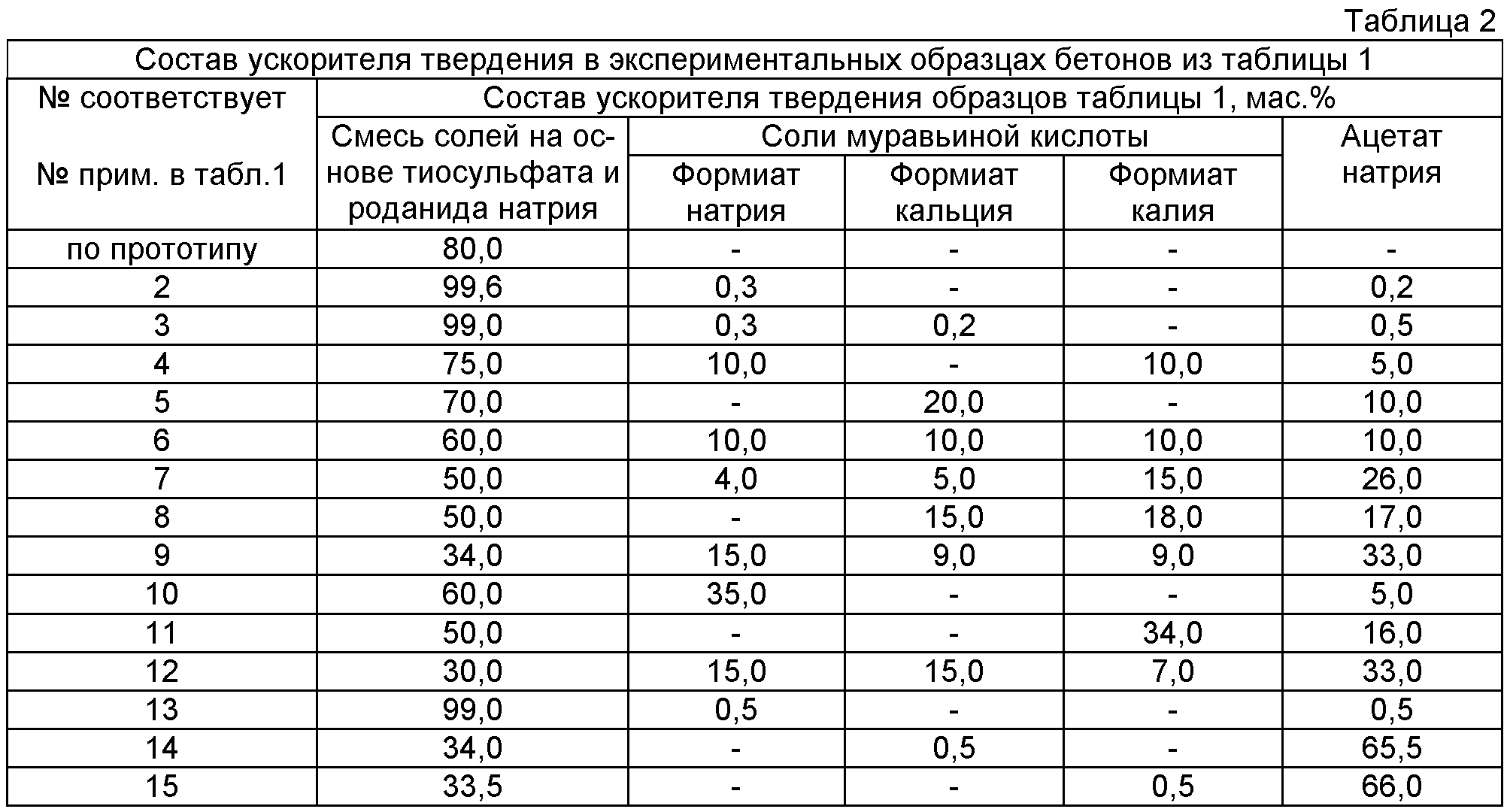 Большое значение имеет именно его раствор. Очень важно запомнить последовательность действий при создании цементно-песчаного раствора.
Большое значение имеет именно его раствор. Очень важно запомнить последовательность действий при создании цементно-песчаного раствора.
Первоначально в емкость добавляют все сухие компоненты, которые затем смешивают. После этого добавляют воду, тщательно следя за тем, чтобы она поступала в небольшом количестве.
Если консистенция раствора уже похожа по тягучести на густую сметану, то воду можно уже не добавлять. Теперь достаточно подождать четверть часа, а затем снова перемешать. Делать это можно с помощью дрели с насадками, главное – следить, чтобы в растворе не образовались комки.
Как только вы убедились в том, что комков нет, следует сразу же приступать к использованию смеси. Постарайтесь уложиться в полчаса, пока не началось твердение отдельных частиц раствора. Если это уже произошло, даже добавление воды уже не поможет.
Расход и процесс отвердевания цементного раствора
Несмотря на то, что цемент не является продуктом питания, не забывайте следить за сроком его годности. Использование старого материала может привести к тому, что прочность кладки или штукатурки будет не на самом высоком уровне. Отвердевает цементно-песчаная смесь при соприкосновении воды и частиц цемента. В этот момент появляется каменеющий со временем гель. Работы по замешиванию и использованию раствора следует проводить в тепле, так как при минусовой температуре отвердевание прекращается совсем.
Использование старого материала может привести к тому, что прочность кладки или штукатурки будет не на самом высоком уровне. Отвердевает цементно-песчаная смесь при соприкосновении воды и частиц цемента. В этот момент появляется каменеющий со временем гель. Работы по замешиванию и использованию раствора следует проводить в тепле, так как при минусовой температуре отвердевание прекращается совсем.
Чтобы подсчитать, сколько потребуется раствора для оштукатуривания, воспользуемся следующими расчетами:
При пропорции 1 к 3 для оштукатуривания 1 кв.м. стены будет использовано 0,02 куб. м. раствора. Таким образом, на 10 квадратных метров площади будет использовано 0,15 куб.м. песка и 0,05 куб.м. цемента.
Впрочем, в подсчетах не учитывается мастерство штукатуров и качество материала.
Нужно купить готовый цементно-песчаный раствор?
Не проблема! Просто позвоните или сделайте заявку по этой ссылке и наши менеджеры свяжутся с вами в ближайшее время!
Эксплуатация, зарядка, хранение аккумуляторной батареи
23. 12.2019
12.2019
Содержание
1. Техническое отступление
2.Основные характеристики аккумуляторных батарей
2.1. Расход воды
2.2. Долговечность батареи
2.3. Рекомендации по эксплуатации
3. Терминология
4. Маркировка АКБ
5. Выбор и покупка АКБ
6. Установка АКБ
7. Рекомендации по эксплуатации и обслуживанию
7.1. Обслуживание АКБ в процессе эксплуатации
7.2. Продление жизни новой батарее
7.3. Зарядка аккумулятора зарядным устройством
8. Особенности эксплуатации АКБ в зимний период
8.1. Прикуривание от другого автомобиля
9. Особенности эксплуатации АКБ в летний период
10. Вопросы безопасности
11. Хранение аккумуляторной батареи
12. Приложения
12.1. Реанимация аккумулятора
12.2. Ещё несколько способов, основанных на использовании электрического тока
Скрыть содержание
1.
 Техническое отступление
Техническое отступление
Назначение автомобильной аккумуляторной батареи понятно каждому мало-мальски сведущему в технических вопросах автолюбителю. С первой ее функцией — обеспечением запуска двигателя — мы сталкиваемся каждый день. Есть и вторая — реже применяемая, но от того не менее значимая — использование в качестве аварийного источника питания при выходе из строя генератора. Кроме того, на современных автомобилях с инжекторным впрыском аккумулятор выполняет роль сглаживателя пульсаций напряжения, выдаваемого генератором. Из этого следует, что следует крайне осторожно относиться к отключению аккумулятора на работающем двигателе. Карбюраторному двигателю ничего не будет, а вот как поведёт себя компьютер, управляющий распределённым впрыском — одному богу известно… Можно загубить компьютер.
Все стартерные батареи, выпускаемые в настоящее время для автомобилей, являются свинцово-кислотными. В основу их работы заложен известный еще с 1858 г., и по сей день остающийся практически неизменным принцип двойной сульфатации.
Как наглядно видно из формулы, при разряде батареи (стрелка вправо) происходит взаимодействие активной массы положительных и отрицательных пластин с электролитом (серной кислотой), в результате чего образуется сульфат свинца, осаждающийся на поверхности отрицательно заряженной пластины и вода. В итоге плотность электролита падает. При зарядке батареи от внешнего источника происходят обратные электрохимические процессы (стрелка влево), что приводит к восстановлению на отрицательных электродах чистого свинца и на положительных — диоксида свинца. Одновременно с этим повышается плотность электролита.
Любая автомобильная батарея представляет из себя корпус — контейнер, разделенный на шесть изолированных ячеек — банок (см. рис.1).
Каждая банка является законченным источником питания напряжением порядка 2.1 В. В банке находится набор положительных и отрицательных пластин, отделенных друг от друга сепараторами. Как известно из школьного курса физики, две разнозаряженные пластины уже сами по себе являются источником постоянного напряжения, параллельное же их соединение увеличивает ток. Последовательное соединение шести банок и дает батарею с напряжением порядка 12.6-12.8 В. Любая из пластин, как положительная, так и отрицательная, есть ни что иное, как свинцовая решетка, заполненная активной массой. Активная масса имеет пористую структуру с тем, чтобы электролит заходил в как можно более глубокие слои и охватывал больший ее объем. Роль активной массы в отрицательных пластинах выполняет свинец, в положительных — диоксид свинца.
Последовательное соединение шести банок и дает батарею с напряжением порядка 12.6-12.8 В. Любая из пластин, как положительная, так и отрицательная, есть ни что иное, как свинцовая решетка, заполненная активной массой. Активная масса имеет пористую структуру с тем, чтобы электролит заходил в как можно более глубокие слои и охватывал больший ее объем. Роль активной массы в отрицательных пластинах выполняет свинец, в положительных — диоксид свинца.
Вес залитой АКБ ёмкостью 55 Ач составляет около 16.5 кг. Эта цифра складывается из массы электролита — 5кг (что соответствует 4,5 л), массы свинца и всех его соединений — 10 кг, а также 1 кг, приходящегося на долю бака и сепараторов.
2. Основные характеристики аккумуляторных батарей
2.0. Электродвижущая сила (ЭДС)
Зависимость ЭДС (грубо говоря, напряжение на выводах аккумулятора) от плотности электролита выглядит так:
Е = 6 * (0,84 + р) , где Е — ЭДС аккумулятора , (В) р — приведенная к температуре 5°С плотность электролита , г/мл
2. 1. Расход воды
1. Расход воды
Показатель, имеющий непосредственное отношение к степени обслуживаемости батареи. Определяется в лабораторных условиях. Батарея считается необслуживаемой, если она имеет очень низкий расход воды в эксплуатации. Необслуживаемые батареи не требуют доливки дистиллированной воды в течении года и более при условии исправной работы регулятора напряжения.
На расход воды прямое влияние оказывает процентное содержание сурьмы в свинцовых решетках пластин. Как известно, сурьма добавляется для придания пластинам достаточной механической прочности. Однако у каждой медали есть обратная сторона. Сурьма способствует расщеплению воды на кислород и водород, следствием чего является выкипание воды и снижение уровня электролита. В батареях предыдущего поколения содержание сурьмы доходило до 10%, в современных этот показатель снижен до 1.5 %.
Панацею от этой беды фирмы видят в освоении т.н. гибридной технологии — замене сурьмы в одной из пластин на кальций. Кальций в решетке является веществом нейтральным по отношению к воде, не снижая при этом механической прочности решеток. А потому разложения воды не происходит и уровень электролита остается неизменным.
А потому разложения воды не происходит и уровень электролита остается неизменным.
Преимущества «кальциевых» АКБ — можно устанавливать в местах , не не требующих удобного доступа для обслуживания. Меньше вероятность выхода из строя из-за коррозии решеток электродов. Лучшие стартерные характеристики.
Недостаток «кальциевых» АКБ — при глубоких разрядах происходит образование нерастворимых солей кальция, и емкость АКБ необратимо теряется. Производители АКБ пытаются устранить этот недостаток добавлением в АКБ серебра и др. компонентов, результат пока окончательно не ясен.
2.2. Долговечность батареи
Средний срок службы современных АКБ при условии соблюдения правил эксплуатации — а это недопущение глубоких разрядов и перезарядов, в том числе по вине регулятора напряжения — составляет 4-5 лет.
Наиболее губительными для батарей являются глубокие разряды. Оставленные на ночь включенными световые приборы, либо другие потребители способны разрядить ее до плотности 1. 12 — 1.15 г/см3, т.е. практически до воды, что приводит к главной беде аккумуляторов — сульфатации свинцовых пластин. Пластины покрываются белым налетом, который постепенно кристаллизуется, после чего батарею практически невозможно восстановить. Отсюда вытекает главный вывод — необходимо постоянно следить за состоянием батареи, периодически замерять плотность электролита. Особенно актуально это в зимнее время. Следует отметить, что сульфатация в определенных пределах — явление нормальное и присутствует всегда. (Вспомните — на основе теории двойной сульфатации построен принцип работы батарей). Но при малом разряде и последующей зарядке батарея легко восстанавливается до исходного состояния. Это возможно и при глубоком разряде батареи, но только в том случае, если следом сразу, же последует заряд. Если же разряжать батарею длительное время, не давая ей «подпитки», то падение плотности, ниже критического значения неизбежно приводит к образованию кристаллов сульфата свинца, не вступающих в реакцию ни при каких обстоятельствах.
12 — 1.15 г/см3, т.е. практически до воды, что приводит к главной беде аккумуляторов — сульфатации свинцовых пластин. Пластины покрываются белым налетом, который постепенно кристаллизуется, после чего батарею практически невозможно восстановить. Отсюда вытекает главный вывод — необходимо постоянно следить за состоянием батареи, периодически замерять плотность электролита. Особенно актуально это в зимнее время. Следует отметить, что сульфатация в определенных пределах — явление нормальное и присутствует всегда. (Вспомните — на основе теории двойной сульфатации построен принцип работы батарей). Но при малом разряде и последующей зарядке батарея легко восстанавливается до исходного состояния. Это возможно и при глубоком разряде батареи, но только в том случае, если следом сразу, же последует заряд. Если же разряжать батарею длительное время, не давая ей «подпитки», то падение плотности, ниже критического значения неизбежно приводит к образованию кристаллов сульфата свинца, не вступающих в реакцию ни при каких обстоятельствах. А это означает, что начался необратимый процесс сульфатации.
А это означает, что начался необратимый процесс сульфатации.
Не менее опасен для батареи и перезаряд. Это происходит при неисправном регуляторе напряжения. При этом электролит начинает «кипеть» — происходит разложение воды на кислород и водород, и понижение уровня электролита. Вот почему необходимо следить за зарядным напряжением. Естественно, это не составляет труда, если на панели приборов присутствует вольтметр. Ну а если его нет? В этом случае также можно довольно просто оценить зарядное напряжение. Для этого запустите и прогрейте двигатель, установив средние обороты и подключите тестер (в режиме вольтметра) между «+» и «массой» аккумуляторной батареи. Нормальный зарядный режим батареи обеспечивается в диапазоне 14±0.5В. Если напряжение меньше — стоит проверить натяжение ремня, надежность контактных соединений цепей системы электроснабжения. Если же это не помогает — неисправность нужно искать в регуляторе напряжения. Впрочем, точно также вина ложится на регулятор, если напряжение превышает 14.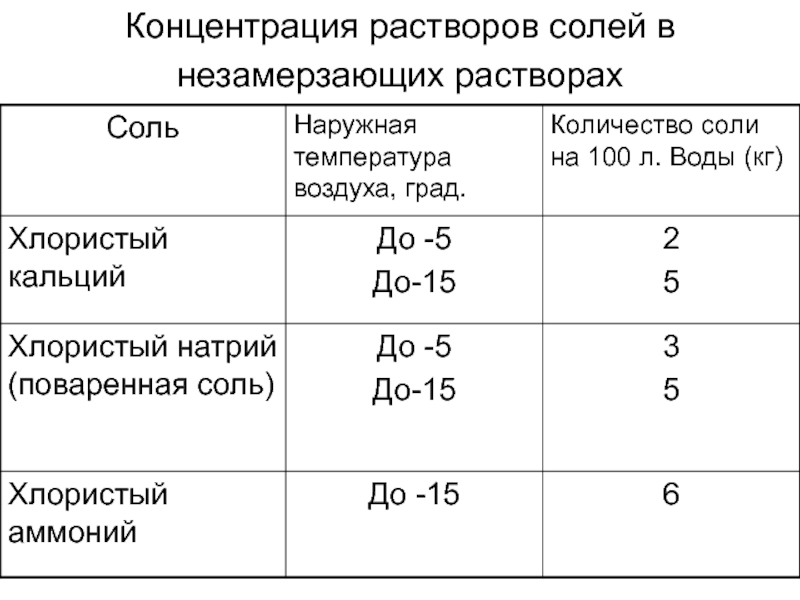 5В.
5В.
В последнее время широкое распространение получили сепараторы карманного типа — т.н. конвертные сепараторы. Их название говорит за себя — в эти конверты помещают одноименно заряженные пластины. Такая конструкция увеличивает срок службы батареи, так как осыпающаяся в процессе эксплуатации активная масса остается в конверте, тем самым предотвращается замыкание пластин.
2.3. Рекомендации по эксплуатации
Батарея, не эксплуатировавшаяся в течении длительного времени (4-5 мес.) нуждается в подзарядке. Связано это с тем, что батареям свойственно такое явление, как саморазряд. На графиках рис.2,3 показаны характеризующие саморазряд величины для различных батарей. В первом случае — это снижение плотности от времени хранения, во втором — падение напряжения.
Впрочем, зачастую подзарядки требует и находящаяся в эксплуатации батарея. Плотность полностью заряженной батареи составляет 1.27- 1.28 г/см3, напряжение — 12.5 В. О степени разряженности батареи судят по плотности электролита.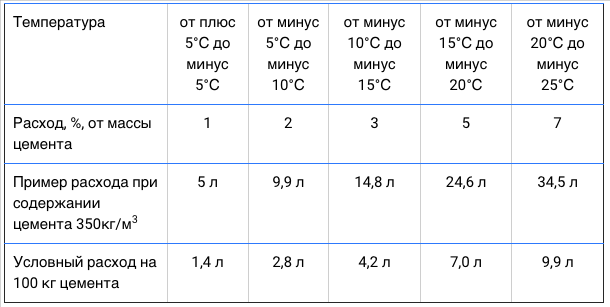 Чем ниже плотность электролита, тем сильнее батарея разряжена. Уменьшение плотности на 0.01 г/см3 по сравнению с номинальной означает, что батарея разрядилась примерно на 6 — 8%. Используя график (см. рис.4) можно оценить зависимость степени разряженности батареи от плотности. Степень разряженности определяют по той банке, в которой плотность электролита минимальная. Всем известна аксиома, тем не менее, позволим повторить ее еще раз — батарею, разряженную летом более чем на 50%, а зимой более чем на 25%, необходимо снять с автомобиля и зарядить. При этом следует помнить, что пониженная плотность зимой более опасна, т.к. кроме всего прочего может привести к замерзанию электролита. Так, при плотности электролита 1.2 г/см3 температура его замерзания составляет около -20°С.
Чем ниже плотность электролита, тем сильнее батарея разряжена. Уменьшение плотности на 0.01 г/см3 по сравнению с номинальной означает, что батарея разрядилась примерно на 6 — 8%. Используя график (см. рис.4) можно оценить зависимость степени разряженности батареи от плотности. Степень разряженности определяют по той банке, в которой плотность электролита минимальная. Всем известна аксиома, тем не менее, позволим повторить ее еще раз — батарею, разряженную летом более чем на 50%, а зимой более чем на 25%, необходимо снять с автомобиля и зарядить. При этом следует помнить, что пониженная плотность зимой более опасна, т.к. кроме всего прочего может привести к замерзанию электролита. Так, при плотности электролита 1.2 г/см3 температура его замерзания составляет около -20°С.
Также необходимо подзарядить батарею, если плотность в разных банках отличается более чем на 0.02 г/см3. Оптимальной является зарядка батареи током, равным 0.05 от ее ёмкости. Для батареи с ёмкостью 55 Ач эта величина составляет 2. 75 А. Чем меньше зарядный ток, тем глубже заряд. Однако не стоит впадать в крайность — при совсем низком токе батарея просто не «закипит», к тому же время зарядки будет несравнимо большим. Наоборот, при очень большом токе батарея «закипит» значительно быстрее, но при этом не успеет зарядиться на все 100%. Признаками окончания зарядки служит бурное выделение газа (т.н. «кипение») и неизменяющаяся на протяжении 1-2 часов плотность электролита.
75 А. Чем меньше зарядный ток, тем глубже заряд. Однако не стоит впадать в крайность — при совсем низком токе батарея просто не «закипит», к тому же время зарядки будет несравнимо большим. Наоборот, при очень большом токе батарея «закипит» значительно быстрее, но при этом не успеет зарядиться на все 100%. Признаками окончания зарядки служит бурное выделение газа (т.н. «кипение») и неизменяющаяся на протяжении 1-2 часов плотность электролита.
Для ориентировочной оценки времени, требуемого на зарядку батареи, можно воспользоваться следующим алгоритмом.
Первоначально, используя график (рис.4) необходимо определить степень разряженности батареи, исходя из реальной плотности АКБ, замеренной ареометром. Далее по степени разряженности определяем потерянную ёмкость (или ёмкость, которую необходимо принять батарее).
Затем, выбрав величину зарядного тока, вычисляем ориентировочное время зарядки по формуле:
Тут следует отметить, что не вся энергия идет на повышение ёмкости. КПД процесса составляет 60-80%, остальное тратится на нагрев, а также связанные с этим электрохимические процессы. Потому реальное время увеличивается примерно в полтора раза от расчетного (что и учитывается коэффициентом «1.5» в формуле).
КПД процесса составляет 60-80%, остальное тратится на нагрев, а также связанные с этим электрохимические процессы. Потому реальное время увеличивается примерно в полтора раза от расчетного (что и учитывается коэффициентом «1.5» в формуле).
Нужно сказать, что использование данного алгоритма оправдано лишь для облегчения процедуры, но ни в коей мере не избавляет от контроля за ходом зарядки. Процесс заряда, а особенно его окончание Вам необходимо контролировать самому, дабы не прозевать начало бурного кипения.
Другой вариант — использование для этих целей автоматических зарядных устройств, отличающихся тем, что зарядка идет при постоянном напряжении, но автоматически изменяющемся в зависимости от степени заряженности батареи токе. При этом зарядное устройство перестает давать ток, если батарея полностью заряжена. Принцип, используемый в подобных устройствах аналогичен зарядке от генератора на автомобиле.
Для примера определим время зарядки батареи ёмкостью 55 Ач током в 5А, плотность которой составляет 1. 25 г/см3. Как видно из графика, при данной плотности батарея разряжена на 25%, что означает потерю ёмкости на величину
25 г/см3. Как видно из графика, при данной плотности батарея разряжена на 25%, что означает потерю ёмкости на величину
Таким образом, примерное время зарядки
Каждодневным способом зарядки батареи является ее заряд от бортовой сети автомобиля (естественно, при условии исправности последней). При данном способе, во первых, невозможен перезаряд, а во-вторых, происходит постоянное перемешивание электролита и наиболее полное его проникновение во внутренние слои активной массы.
Однако было бы ошибочным полагать, что заряд батареи начинается сразу же после пуска двигателя и продолжается все время, пока двигатель в работе. Исследования показывают, что батарея начинает принимать заряд только после прогрева электролита до положительной температуры, что при эксплуатации в зимних условиях происходит примерно через час после начала движения. Именно этим и опасен довольно распространенный, по крайней мере, в нашем автомобильном городе, способ эксплуатации транспортных средств. Холодный запуск зимой с получасовым движением до работы, и затем редкие непродолжительные поездки на протяжении рабочего дня не дают прогреться электролиту и, следовательно, зарядиться Вашей батарее. Тем самым разряженность АКБ увеличивается изо дня в день и в итоге может привести к печальному результату. Из этого следует, что зимой необходимо проверять состояние АКБ и своевременно подзаряжать ее регулярно
Холодный запуск зимой с получасовым движением до работы, и затем редкие непродолжительные поездки на протяжении рабочего дня не дают прогреться электролиту и, следовательно, зарядиться Вашей батарее. Тем самым разряженность АКБ увеличивается изо дня в день и в итоге может привести к печальному результату. Из этого следует, что зимой необходимо проверять состояние АКБ и своевременно подзаряжать ее регулярно
Физические процессы, происходящие при пуске двигателя, отличаются от процессов при разряде батареи потребителями. При пуске участвует не весь объем активной массы и электролита, а лишь та ее часть, которая находится на поверхности пластин и соприкасающийся с поверхностью пластин электролит. Поэтому, после неудачной попытки запустить двигатель, следует подождать некоторое время для того, чтобы электролит перемешался, плотность его выровнялась, он проник в поры активной массы. Нормальный запуск двигателя при однократном вращении стартера в течении 10с забирает ёмкость 300А х 10с = 3000 Ас = 0. 83 Ач, что составляет около 1.5% от ёмкости аккумулятора.
83 Ач, что составляет около 1.5% от ёмкости аккумулятора.
При медленном же разряде участвуют не только поверхностные слои активной массы, но и глубинные, потому и разряд происходит более глубокий. Однако это не означает, что стартерные режимы не так губительны для батареи — стартером точно также можно разрядить батарею до критической величины.
Каковы же признаки выхода из строя батареи? Батарея не заряжается, плотность низкая и не повышается в процессе заряда. Большой саморазряд — батарея зарядилась, но не держит заряд. Можно попытаться потренировать батарею, однако если произошло осыпание активной массы пластин, либо кристаллизация сульфата свинца, то это уже не исправить.
Вообще, освоить способ оценки степени возможной разрядки батареи от каких-либо действий (в том числе и осознанных) не составит большого труда. Необходимо усвоить несколько истин и запомнить несколько цифр.
Батарея начинает принимать заряд лишь только после прогрева электролита до положительной температуры (как вы понимаете, при температуре воздуха -20°С температура электролита в батарее хранящегося на свежем воздухе автомобиля будет примерно такой же. )
)
Коэффициент полезного действия процесса зарядки составляет примерно 50%.
Каждый автомобильный генератор характеризуется следующими показателями:
ток отдачи генератора при работе двигателя на холостом ходу.
ток отдачи генератора при работе двигателя на номинальных оборотах.
Для ВАЗовских автомобилей эти цифры имеют следующие значения:
Таблица 1
Модель автомобиля…………………..2101-2106……2108-2109……2110
ток отдачи на холостом ходу…………….16………………24…………..35
ток отдачи на номинальных оборотах 42……………….55…………..80
Как видно из таблицы, на последних моделях автомобилей Волжского автозавода устанавливаются генераторы, имеющие характеристики тока отдачи, в два раза превосходящие по величине характеристики генераторов первых моделей.
И наконец, примерное потребление энергии автомобильными потребителями:
Таблица 2
потребитель……….ток, А (приблизительно)
зажигание. …………….2
…………….2
габариты……………….4
ближний свет…………9
дальний свет………..12
обогрев стекла……10-11
стеклоподьемник…20-30
вентилятор отопителя:
1-я скорость…………5-7
2-я скорость……….10-11
стеклоочистители…3-5
магнитола…………….5
ИТОГО……………….38-48
Таким образом, оставленные включенными габариты за три часа «съедят» 4А х 3ч= 12 Ач ёмкости батареи, что соответствует разряду приблизительно на 20%. Это не страшно для одного раза. Однако повторив это ещё раз, Вы уже рискуете не завести свою машину, особенно, если дело происходит зимой, т.к. разряд составит порядка 40% (тем более, что к тому же зимой батареи, как правило, эксплуатируются заряженными далеко не на 100%).
Аналогично можно прикинуть, что Вы имеете при продолжительной работе двигателя на холостом ходу. Как уже показано выше, ток отдачи генератора автомобиля ВАЗ-2108 на холостом ходу составляет 24А. Вычитаем из этой величины 2А, необходимые для обслуживания системы зажигания. Остается 22А. Используя таблицу 2, нетрудно прикинуть, что можно включать с тем, чтобы хоть немного досталось бы и аккумулятору (при этом помните про КПД зарядки, составляющий 50%).
Вычитаем из этой величины 2А, необходимые для обслуживания системы зажигания. Остается 22А. Используя таблицу 2, нетрудно прикинуть, что можно включать с тем, чтобы хоть немного досталось бы и аккумулятору (при этом помните про КПД зарядки, составляющий 50%).
Для владельцев иномарок с автоматической коробкой передач картина ещё более сложная. Обычно, стоя в пробке или на светофоре, Вы не переключаетесь на нейтраль, а давите ногой на тормоз. Это понижает обороты двигателя от стандартных 800-900 об./мин. до 600-700 об./мин., что, соответственно понизит ток, выдаваемый генератором, а стоп-сигналы добавят ещё пару ампер потребления тока. Да и обогрев заднего стекла у немцев, например, существенно мощнее, чем у отечественных автомобилей.
Следует знать, что зимние условия эксплуатации автомобиля в принципе очень тяжелы для аккумуляторной батареи. Наверняка будут полезны следующие данные. Результаты проводимых в ГДР исследований говорят о том, что при эксплуатации автомобиля в очень тяжелых условиях (испытания по так называемому режиму «город-зима-ночь») аккумулятор получает порядка 1Ач в час
3.
 Терминология
Терминология
Аккумуляторная батарея — один из основных элементов электрооборудования автомобиля, поскольку она накапливает и хранит электроэнергию, обеспечивает запуск двигателя в различных климатических условиях, а также питает электроприборы при неработающем двигателе.
Автомобильные свинцово-кислотные 12-вольтовые АКБ состоят из 6-ти последовательно соединенных элементов (банок), объединенных в общий корпус. Каждая банка имеет газоотвод, конструкции которого могут существенно отличаться.
Электролит представляет собой раствор серной кислоты в дистиллированной воде (для средней полосы России плотностью 1.27-1.28 г/см3 при t=+20°С). Кипение электролита — бурное выделение газа при электролитическом разложении воды с выделением кислорода и водорода. Это происходит во время заряда батареи.
Саморазряд — самопроизвольное снижение ёмкости АКБ при бездействии. Скорость саморазряда зависит от материала пластин, химических примесей в электролите, его плотности, от чистоты верхней части корпуса батареи и продолжительности ее эксплуатации.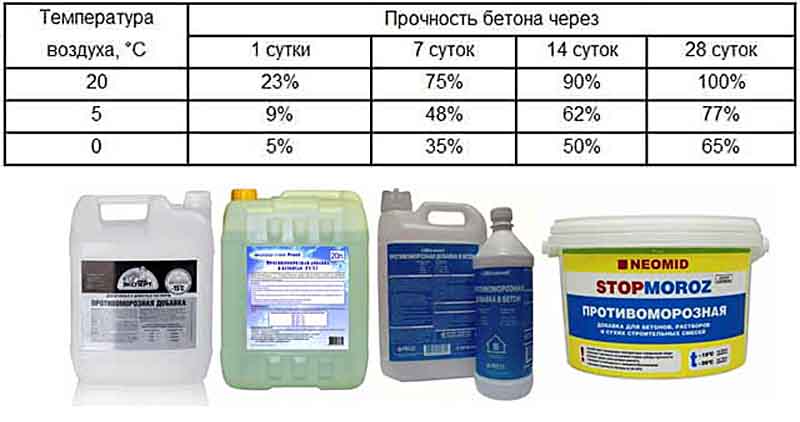
Напряжение полностью заряженной аккумуляторной батареи без нагрузки (ЭДС — электродвижущая сила) должно находиться в пределах 12.6-12.9 В. Напряжение в бортовой сети автомобиля при работающем двигателе несколько выше, чем на клеммах АКБ, и должно находиться в пределах 14.0-14.2 В (0,2 В от крайних значений). Значение напряжения ниже 13.8 В ведет к недозаряду батареи, а выше 14.4В — к перезаряду, что одинаково пагубно сказывается на ее сроке службы.
Полярность аккумуляторной батареи — термин, определяющий расположение токосъемных выводов на ее корпусе. На зарубежных батареях полярность может быть прямой или обратной, т. е. ориентировка положительного и отрицательного выводов относительно корпуса может быть различной. По российскому стандарту (если смотреть со стороны выводов) отрицательный (-) должен располагаться справа, положительный (+) слева.
Емкость батареи — способность батареи принимать и отдавать энергию — измеряется в ампер-часах (Ач). Для оценки ёмкости батареи принята методика 20-ти часового разряда током 0. 05С20 (т.е. током, равным 5% от номинальной ёмкости). Т.е., если ёмкость батареи 55Ач, то разряжая ее током 2.75 А, она полностью разрядится за 20 часов. Аналогично для батарей ёмкостью 60Ач полный 20-ти часовой разряд произойдет при чуть большем токе разряда — 3А.
05С20 (т.е. током, равным 5% от номинальной ёмкости). Т.е., если ёмкость батареи 55Ач, то разряжая ее током 2.75 А, она полностью разрядится за 20 часов. Аналогично для батарей ёмкостью 60Ач полный 20-ти часовой разряд произойдет при чуть большем токе разряда — 3А.
Данная характеристика определяет возможность питать потребителей в экстремальной ситуации (при отказе генератора). Характеризуется объемом активной массы.
Значение тока холодного старта при -18°С (по DIN) — Величина тока, которую батарея способна отдать при пуске двигателя при температуре -18°С. Наиболее важная характеристика, напрямую сказывающаяся на пуске двигателя. Ведь при -20°С ток, потребляемый стартером, составляет порядка 300А. (Для пуска в летнее время горячего двигателя этот же показатель равен 100-120А.) Значение стартового тока определяется конструкцией батареи, пластин, сепараторов. Сепараторы карманного типа без каких-либо других дополнений увеличивают напряжение батареи на 0.3В, одновременно улучшая стартовые характеристики. Чем ниже внутреннее сопротивление батареи, тем выше стартовый ток, тем надежнее пуск двигателя при низких температурах.
Чем ниже внутреннее сопротивление батареи, тем выше стартовый ток, тем надежнее пуск двигателя при низких температурах.
Резервная ёмкость — время, в течении которого батарея сможет обеспечить работу потребителей в аварийном режиме. Величина резервной ёмкости, выраженная в минутах, последнее время все чаще проставляется изготовителями батарей после значения тока холодного старта.
Корпус современных АКБ изготавливается из пластмассы, в большинстве случаев полупрозрачной, позволяющей контролировать уровень электролита.
Необслуживаемые батареи. Сразу следует оговориться, что этот термин не должен пониматься буквально и восприниматься как руководство к бездействию. Это название говорит об улучшенных потребительских свойствах батареи. Необслуживаемые АКБ требуют долива воды не чаще одного раза в год при условии использования их на автомобилях с исправным электрооборудованием и среднегодовым пробегом 15-20 тыс. км. Встречаются конструкции, исключающие всякое вмешательство на всем протяжении срока службы, но они особенно критичны к состоянию автомобильного электрооборудования.
Большинство необслуживаемых батарей выпускаются заводами-изготовителями, залитыми электролитом. Так как эти батареи имеют значительно меньший саморазряд, они могут храниться от 6 месяцев до 1 года без подзаряда. Саморазряд новых необслуживаемых батарей за 12 месяцев может составить до 50% от номинальной ёмкости.
4. Маркировка АКБ
На современные аккумуляторные батареи наносится следующая маркировка:
Некоторые батареи имеют такую маркировку:
Несмотря на то, что после ёмкости стоит значение 280А, цифра, интересующая нас и показывающая ток холодного старта по принятому у нас стандарту DIN равна 255А.
Обозначения основных характеристик на батареях различных производителей отличаются друг от друга. Большинство европейских производителей и значительная их часть в Азии руководствуются промышленным стандартом Германии DIN 43539 часть 2, который оговаривает два основных параметра: ёмкость батареи, измеряемую в ампер-часах (Ач) при +25°С, и ток стартерного разряда в амперах (А) при -18°С.
Батареи американских производителей испытываются по требованию американского стандарта SAE J537g, который включен в международный стандарт BCI и также вводит два основных параметра: резервную ёмкость, измеряемую в минутах при +27°С, и ток холодной прокрутки — в амперах при -18С. Стандарт SAE не предусматривает измерение ёмкости батареи в ампер-часах.
Первый рассматривает способность батареи к длительным разрядам меньшими токами, второй — разряд большими токами, но за меньший отрезок времени.
Пересчет значения тока стартерного разряда по европейскому стандарту DIN в ток холодной прокрутки по американскому стандарту SAE может производиться с помощью экспериментальных коэффициентов. Для батарей ёмкостью до 90Ач используется коэффициент 1.7, т. е. ISAE = 1.7 IDIN. Для батарей ёмкостью от 90 до 200 Ач используется коэффициент 1.6, т. е. ISAE = 1.6 IDIN.
В настоящее время в Европе наряду с немецким стандартом DIN введен новый единый стандарт En — 60095-1/93.
Кроме того, на необслуживаемых батареях проставляется соответствующая надпись. Чаще всего на русском, английском или немецком языке (либо на языке производителя, как например, на испанских батареях «Tudor»).
Чаще всего на русском, английском или немецком языке (либо на языке производителя, как например, на испанских батареях «Tudor»).
5. Выбор и покупка АКБ
Убедитесь, что выбираемая батарея соответствует конструктивным особенностям вашего автомобиля (ёмкость, место установки, способ крепления, полярность, форма и размер токосъемных выводов). Специализированные торговые фирмы имеют каталоги всего ассортимента, в которых систематизирована информация о модификациях и технических характеристиках.
Нецелесообразно на автомобиль с устаревшей системой электрооборудования устанавливать батарею, исключающую долив воды. Это приведет к сокращению ее срока службы или отказу.
Емкость батареи не должна существенно отличаться от указанной заводом-изготовителем автомобиля. Несоблюдение этого условия приводит к резкому сокращению службы, как батареи, так и стартера.
Очень неплохо знать рекомендуемую величину пускового тока для Вашего автомобиля. На многих (японских) автомобилях устанавливаются стартёры с редуктором. Это позволяет существенно уменьшить величину пускового тока, а значит существенно продлить жизнь Вашего аккумулятора.
Это позволяет существенно уменьшить величину пускового тока, а значит существенно продлить жизнь Вашего аккумулятора.
Внимательно изучите текст гарантийного талона. Обратите особое внимание на те разделы, где перечислены: случаи, исключающие гарантийное обслуживание; адреса гарантийных мастерских; условия эксплуатации.
Маркировка аккумулятора должна иметь ссылку на стандарт (DIN, SAE, En или другие). В маркировке по стандарту SAE не указывается значение ёмкости в ампер-часах (Ач). Указание ёмкости в Ач в стандарте SAE – косвенный признак подделки. Наиболее подвержены подделкам дорогие аккумуляторы известных фирм-изготовителей, поэтому приобретать их лучше в торговых фирмах, заслуживающих доверие.
Большинство фирм-изготовителей кодирует дату выпуска АКБ. Современные необслуживаемые батареи допускают достаточно длительное хранение без существенной потери своих потребительских свойств, поэтому дата изготовления менее актуальна. Предпочтительнее приобретать залитый качественным заводским электролитом аккумулятор. Он готов к работе, легко поддается проверке. Не залитый сухозаряженный аккумулятор требует дополнительного времени и затрат на подготовку к эксплуатации.
Он готов к работе, легко поддается проверке. Не залитый сухозаряженный аккумулятор требует дополнительного времени и затрат на подготовку к эксплуатации.
Не спешите отдать деньги! Вы вправе требовать проверки аккумулятора. Первым делом сдерите с него защитную упаковочную пленку, какой бы красивой она ни была, и убедитесь, что корпус не поврежден – такое случается довольно часто. Затем попросите продавца измерить плотность электролита – она не должна быть ниже номинальной более чем на 0,02 г/см3 и одинаковой во всех банках, что соответствует примерно 80-процентной заряженности батареи. Последнюю проверку следует провести с нагрузочной вилкой – ее вольтметр должен показать 12.5–12.9 В при отключенной нагрузке, а при включенной – не опускаться в течение 10 секунд ниже 11В.
В случае отклонения от этих значений, батарея может оказаться частично или полностью непригодной к эксплуатации.
Если вам отказывают в проверке аккумулятора, не могут подтвердить качество товара сертификатом, гарантийным талоном, то лучше отказаться от покупки.
6. Установка АКБ
Перед установкой батареи обязательно полностью удалите с нее полиэтиленовую пленку. Газоотводные отверстия должны быть открытыми. Обратите внимание на правильность подключения. Клеммы АКБ рекомендуется зачистить и после закрепления смазать Литолом-24. Это делается для предохранения контактов от попадания влаги и окисления места контактов. Особенно это касается силовых проводов с медными (а не свинцовыми) наконечниками.
Очень важно уделить внимание проводам. Клеммы необходимо зачистить не только со стороны аккумулятора, но и с другой стороны. Место, куда крепится массовый провод (-) надо тоже тщательно зачистить от краски, масла и прочей грязи. Контакт затянуть туго. Это же касается клеммы на стартёре. Невнимание к проводам и контактам может очень сильно «выйти боком» зимой на морозе.
Батарея должна стоять на своём месте жёстко. Болтание её в крепёжных элементах недопустимо. Дополнительная вибрация скажется на долговечности батареи. Замыкание и осыпание пластин в банках чаще всего происходят именно из-за вибрации.
Замыкание и осыпание пластин в банках чаще всего происходят именно из-за вибрации.
Обратите внимание, что на многих автомобилях батарея стоит довольно близко к выпускному коллектору. То есть летом ей будет довольно жарко, а это для батареи очень плохо! На «правильных» машинах предусмотрена термоизоляция АКБ от двигателя.
7. Рекомендации по эксплуатации и обслуживанию
Условия эксплуатации оказывают существенное влияние на срок службы аккумуляторной батареи. Частые запуски двигателя и поездки на короткие расстояния, неисправности электрооборудования (стартер, генератор, реле-регулятор), дополнительные потребители электроэнергии, несвоевременное обслуживание, ненадежное крепление батареи способны сильно сократить срок ее службы.
При продолжительном движении по трассе батарея может перезаряжаться (кипеть) — в городе с малыми пробегами и «пробками» она, как правило, разряжается (см. выше).
Генератор (при холостых оборотах двигателя) не обеспечивает работу большинства штатных потребителей, не говоря о дополнительных. Зимой ситуация усугубляется. К включенным габаритным огням, ближнему свету фар, стоп-сигналам, указателям поворота, аудиоаппаратуре добавляются обогрев заднего стекла и вентилятор отопителя. Ежедневный недозаряд батареи постепенно уменьшает ее ёмкость, что в итоге приводит к невозможности запуска двигателя стартером.
Зимой ситуация усугубляется. К включенным габаритным огням, ближнему свету фар, стоп-сигналам, указателям поворота, аудиоаппаратуре добавляются обогрев заднего стекла и вентилятор отопителя. Ежедневный недозаряд батареи постепенно уменьшает ее ёмкость, что в итоге приводит к невозможности запуска двигателя стартером.
Отказ аккумуляторной батареи может быть вызван и током утечки в электрооборудовании автомобиля. Это происходит, когда при отключении всех потребителей один или часть из них остается включенным в электрическую цепь (неисправны выключатель или реле). Виновником может быть и сигнализация. После глубокого разряда АКБ может не восстановить свою первоначальную номинальную ёмкость. Батарея не сможет нормально работать, если для запуска двигателя требуется продолжительное включение стартера (неисправны системы питания, зажигания).
7.1. Обслуживание АКБ в процессе эксплуатации сводится к проверке и приведению в соответствие с требованиями: уровня и плотности электролита; чистоты и надежности крепления электрических соединений батареи с корпусом автомобиля, параметров электрооборудования, крепления батареи. Необходимо также следить за правильным натяжением ремня генератора, очищать и смазывать выводы и клеммы, содержать батарею в чистоте. Протирайте верхнюю поверхность водным раствором питьевой соды. Доведение плотности электролита до требуемой производится путем заряда батареи от стационарного зарядного устройства.
Необходимо также следить за правильным натяжением ремня генератора, очищать и смазывать выводы и клеммы, содержать батарею в чистоте. Протирайте верхнюю поверхность водным раствором питьевой соды. Доведение плотности электролита до требуемой производится путем заряда батареи от стационарного зарядного устройства.
Значение зарядного тока в амперах (А) не должно превышать 1/10 ёмкости батареи (упрощенно).
7.2. Продление жизни новой батарее
Коротко об этом сказать трудно. В первую очередь, следует залить электролит, точно соответствующий не только климатической зоне, но и сезону эксплуатации. Если батарея будет работать только в теплое время года, то плотность электролита может быть 1.20 г/см3, а если до -15°С — 1.24 г/см3 и т.д. Такая точность, безусловно, снизит скорость сульфатации пластин, следовательно, увеличит долговечность батареи.
На срок службы АКБ значительно влияет средняя степень заряженности, которая зависит от исправности реле-регулятора. Необходимо, чтобы эта величина поддерживалась не ниже 75%.
Необходимо, чтобы эта величина поддерживалась не ниже 75%.
справка:
Установлено, что отклонение регулируемого напряжения на 10…12% вверх или вниз от оптимального сокращает срок службы батареи в 2…2.5 раза.
Во-первых, отрегулируйте двигатель так, чтобы он легко заводился с пол-оборота. Это предохранит АКБ от глубокого разряда. При пуске двигателя стартером через аккумуляторную батарею проходит ток в несколько сот Ампер, что не способствует ее долговечности. Поэтому, чем легче пуск двигателя, тем лучше для АКБ: она прослужит дольше.
справка:
Сокращение времени работы стартера вдвое при шести-восьми ежедневных пусках повышает срок службы аккумуляторной батареи приблизительно в 1.5 раза.
Во-вторых, отрегулируйте при необходимости реле-регулятор, чтобы напряжение было в пределах 13.8…14.4В. Это одно из важнейших условий. В-третьих, никогда не позволяйте снизиться уровню электролита в банках ниже требуемого.
справка:
Несвоевременная доливка в аккумуляторы дистиллированной воды может снизить срок службы батареи на 30%.
Эти простые советы, продлят жизнь АКБ.
Кроме этого, специалисты советуют при наличии зарядного устройства при любой возможности (например, на ночь) ставить аккумуляторную батарею на подзарядку малым током — около 1…2А. Для этого можно АКБ не снимать с автомобиля. Только эта операция, если ее проделывать регулярно, не реже одного раза в месяц, увеличивает срок службы батареи, по крайней мере, на год.
7.3. Зарядка аккумулятора зарядным устройством
Ну а теперь как заряжать? Зарядные устройства бывают с ручной и автоматической регулировкой (Орион PW-270, Орион PW-320) или автоматические (все остальные зарядные устройства Орион). Перед зарядкой необходимо открыть все газовые каналы: вывернуть пробки, снять крышки банок.
При зарядке важны три параметра: напряжение, ток зарядки и время. Когда аккумулятор частично процентов на 25 разряжен, то начальный ток заряда при включении выпрямителя может резко скакнуть вверх. Отрегулируйте его на зарядный ток около 1/10 ёмкости аккумулятора или меньше (это общепринятое правило заряда кислотных батарей).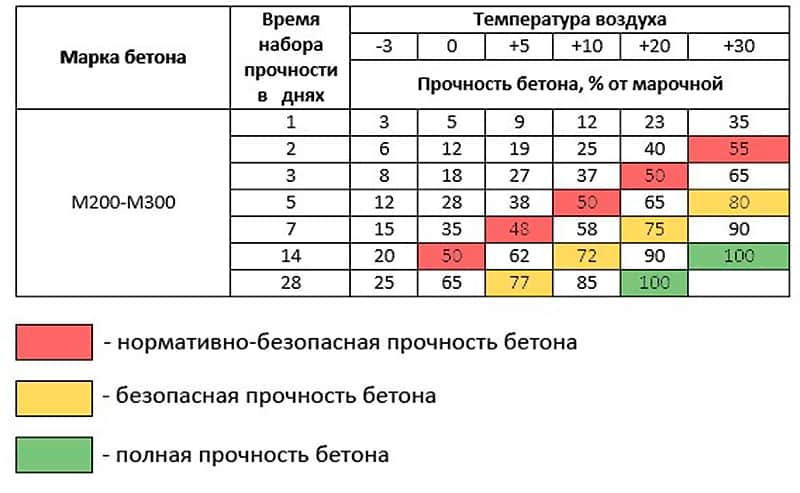 Т.е., если у Вас батарея имеет маркировку 55Ah — выставляем ток около 5.5А.
Т.е., если у Вас батарея имеет маркировку 55Ah — выставляем ток около 5.5А.
Если необходимо зарядить батарею в кратчайшее время, можно выставить и больший ток. В соответствии с законом Вудбриджа который гласит: сила зарядного тока (в амперах) не должна превышать величину заряда (в ампер-часах), недостающего до полной ёмкости акуммулятора. При этом зарядное устройство должно автоматически снижать ток при повышении напряжения или выключаться при достижении порогового напряжения на батарее. В противном случае (если ЗУ этого не делает) необходимо непрерывно контролировать зарядный ток и напряжение в ручную.
Далее в процессе зарядки напряжение будет расти, а ток уменьшаться. Считается, если ток не уменьшается в течение последних 2-3 часов, то аккумулятор заряжен. Важно помнить, что нельзя вести заряд большим током более 25 часов. Электролит сильно нагреется и выкипит, пластины от нагрева может повести и они замкнут друг на друга. Обычно нормальное время полного заряда около 15 часов.
Иногда необходимо выровнять плотность небольшим током. Например, если плотность электролита в разных банках 1.23, 1.25. Включив зарядное устройство, устанавливаем ток зарядки порядка 1-2А. Данное значение у разных АКБ- разное и зависит от многих факторов: конструкции, пассивационного материала пластин, состояния батареи и т.д. Время такой зарядки до двух суток. Особенно это необходимо делать после того, как аккумулятор разряжен в ноль бесплодными попытками завести двигатель. При чём, делать это надо сразу, пока не началась сульфатация пластин.
Батареи, исключающие долив воды, должны заряжаться только устройствами с автоматическим поддержанием зарядного напряжения. Несоблюдение этого условия приведет к снижению их срока службы. Конкретные требования по режиму заряда, эксплуатации и обслуживанию должны быть изложены в инструкции или гарантийном талоне, прилагаемом к батареям.
В настоящее время разные производители обозначают разное напряжение окончания заряда. Как правило, оно составляет от 15 до 16В (для батарей устаревших конструкций, с применением в качестве пассивирующего материала сурьмы — меньше). На самом деле, порог ограничения напряжения автоматического зарядного устройства 15 или 16 вольт (для батареи с прописанными, для полного заряда, 16ю вольтами, например Varta) влияет только на время заряда последних 2-4% емкости.
Как правило, оно составляет от 15 до 16В (для батарей устаревших конструкций, с применением в качестве пассивирующего материала сурьмы — меньше). На самом деле, порог ограничения напряжения автоматического зарядного устройства 15 или 16 вольт (для батареи с прописанными, для полного заряда, 16ю вольтами, например Varta) влияет только на время заряда последних 2-4% емкости.
Для доведения уровня электролита до нормы недопустимо использовать электролит! В аккумуляторную батарею доливают только дистиллированную воду. Не используйте воду сомнительного происхождения. При частом выкипании проверьте электрооборудование автомобиля.
Необходимо знать, что при сильном снижении уровня электролита внутри корпуса аккумулятора может образоваться опасная концентрация газовой смеси. Чтобы исключить вероятность взрыва, нельзя подносить к батарее открытое пламя (даже сигарету) и допускать искрение электроконтактов. Системы газоотвода некоторых современных батарей более взрывобезопасны. В средней полосе России АКБ не требуют корректировки плотности электролита при смене сезонов.
В средней полосе России АКБ не требуют корректировки плотности электролита при смене сезонов.
Перед зимней эксплуатацией автомобиля сделайте обслуживание не только аккумуляторной батареи (см. выше), но и систем, влияющих на запуск двигателя. Обязательно залейте моторное масло, соответствующее сезону. Для облегчения запуска двигателя в сильные морозы занесите батарею на несколько часов в теплое помещение.
Перед длительной зимней стоянкой также обслужите батарею, но не храните ее в теплом помещении, а оставьте на автомобиле со снятыми клеммами. Чем ниже температура, тем меньше скорость ее саморазряда.
Недопустимо оставлять на морозе разряженную батарею. Электролит низкой плотности замерзнет, и кристаллы льда приведут ее в негодность. Плотность электролита разряженного аккумулятора может снизиться до 1,09 г/см3, что приведет к его замерзанию уже при температуре -7°С. Для сравнения – электролит плотностью 1.28 г/см3 замерзает при t=-65°С.
Опрокидывание аккумуляторной батареи и слив электролита могут привести к замыканию пластин и выходу ее из строя.
Для борьбы с паразитными токами утечки введите себе привычку вытирать корпус батареи насухо от всякой нечисти. Если совсем в лом, то хотя бы делайте чистый круг вокруг плюсовой клеммы, чтобы разорвать паразитные электрические связи. Ну, а если Вы любите свою машину, то разведите немного соды в воде и протрите всю поверхность корпуса батареи и вытрете ее насухо. Все тряпки, которые прикасались к аккумулятору выбросить немедленно! А заодно проверите крепление батареи, уровень электролита и его плотность. Времени это займёт минут 10-15, а сэкономить может часы и кучу нервов.
8. Особенности эксплуатации АКБ в зимний период
Перво-наперво замерим плотность электролита во всех банках без исключения. Норма 1.27-1.28 г/см3. У Вас далеко не так? Значит, снимаем батарею и ставим на зарядку. И это однозначно! Ни в коем случае не пытаемся повысить плотность электролита добавлением концентрированной кислоты, какая бы низкая не была его плотность. Желаемого же результата — повышения ёмкости батареи при этом не произойдет.
Далее. Обязательно провести ревизию всех силовых проводов, клемм и контактов. Клеммы зачистить мелкой шкуркой. Контакты на АКБ тоже зачистить и затянуть. Можно затем смазать литолом, чтобы к контактам не попадала влага. С другой стороны силовых проводов так же провести ревизию контактов.
8.1. Прикуривание от другого автомобиля
Для российских автовладельцев нормальная ситуация, когда сосед просит «прикурить» его аккумулятор. Для этой нехитрой процедуры помимо автомобиля с заряженным аккумулятором, необходимы ещё и правильные провода. Не забываем, что по этим проводам у нас потечёт около 200 ампер!
На что нужно обратить внимание при покупке:
1. Толщина жилы медного провода. Сняв изоляцию с крокодила (зажима) можно увидеть саму жилу. Чем толще, тем лучше. Не обращайте внимание на толщину кабеля. Главное проводник тока, а не толщина изоляции.
2. Надежность крепления жилы к крокодилу провода прикуривателя. Медная жила д.б. облужена, затем обжата и припаяна. Если эти условия соблюдены, то потерь в месте соединения будет меньше. Все стартовые провода Орион 100% паяются.
Если эти условия соблюдены, то потерь в месте соединения будет меньше. Все стартовые провода Орион 100% паяются.
3. Изоляция. Лучший вариант — морозоустойчивая резина или силикон. Зимой такие провода остануться эластичными.
4. Длинна проводов. Провода по длинне нужно выбирать не длинее, чем нужно.
5. Крокодилы (зажимы). При покупке обращайте внимание на толщину стали из которой они сделаны и силу пружины, а не габаритные размеры.
Чтобы не навредить сложным электронным системам вашей собственной машины, эта, казалось бы, элементарная процедура требует соблюдения строгой последовательности действий.
1. Соедините красный кабель с клеммой (+) на заряженном аккумуляторе.
2. Соедините другой конец красного кабеля с клеммой (+) на «севшем» аккумуляторе.
3. Соедините черный кабель с клеммой (-) на заряженном аккумуляторе.
4. Соедините другой конец черного кабеля с чистой точкой заземления на блоке двигателя или на шасси, главное — подальше от аккумулятора, карбюратора, топливных шлангов и т. п. В момент подсоединения будьте готовы к небольшой искре.
п. В момент подсоединения будьте готовы к небольшой искре.
5. Следите, чтобы оба кабеля не касались движущихся деталей.
6. Попробуйте запустить автомобиль с «севшим» аккумулятором. Если двигатель не заведется, подождите несколько минут и повторите попытку. Если же заведется, дайте ему поработать несколько минут в таком положении. Если не заведется повторите попытку через 2-3 минуты.
7. При отсоединении кабеля следуйте описанной выше процедуре в обратной последовательности.
8.2 Запуск машины при помощи предпускового зарядного устройства Вымпел. Подключаете устройство, выставляете максимальный ток 18А, оживляете акумулятор в течении 10-15 мин. Затем не отключая зарядного устройства пробуете завести. Если не получилось повторяете попытку заново.
9. Особенности эксплуатации АКБ в летний перио
д
Не удивляйтесь, если однажды вам будет трудно или вообще не завести машину в жаркую погоду. Теплое время года — такое же испытание, как и холод. Тепло ускоряет химические процессы. Неисправности и дефекты электрической системы автомобиля или аккумулятора незамедлительно скажутся на состоянии батареи. Но, скорее всего, узнаете вы об этом в самый неподходящий момент. Например, ночью во время дождя, когда придется включить освещение, вентиляцию и стеклоочистители. Поэтому не расслабляйтесь. Лето — самый подходящий период для покупки нового аккумулятора.
Тепло ускоряет химические процессы. Неисправности и дефекты электрической системы автомобиля или аккумулятора незамедлительно скажутся на состоянии батареи. Но, скорее всего, узнаете вы об этом в самый неподходящий момент. Например, ночью во время дождя, когда придется включить освещение, вентиляцию и стеклоочистители. Поэтому не расслабляйтесь. Лето — самый подходящий период для покупки нового аккумулятора.
Летом автомобилист не сразу заметит, что в аккумуляторе плотность электролита и его уровень в банках недостаточные. Но чем выше температура окружающей среды, тем активнее электрохимические процессы. В результате электролиза кислород вступает во взаимодействие с пластинами, а ставший свободным водород испаряется. Таким образом, из электролита исчезает вода. Как только уровень раствора оказывается ниже уровня пластин, начинается сульфатация пластин (сульфат свинца растворяется в электролите, а затем оседает на поверхности пластин уже в виде крупных нерастворимых кристаллов и происходит изоляция пластин от электролита). Емкость батареи уменьшается. Электрохимические реакции останавливаются. Аккумулятор выходит из строя.
Емкость батареи уменьшается. Электрохимические реакции останавливаются. Аккумулятор выходит из строя.
Имейте в виду, что во время длительного хранения аккумулятора происходит саморазряд (снижение ёмкости). Оставлять батарею в разряженном состоянии не рекомендуется: в этом случае вода испаряется, и открываются пластины. А дальше все, как описано выше.
Саморазряд увеличивается от высокой температуры, грязи и электролита (воды) на крышке батареи. Еще одна причина возникновения паразитных токов — неодинаковая плотность электролита в разных банках и на разных уровнях. Это может произойти после доливки большого количества воды. Чтобы избежать неприятностей, зарядите аккумулятор или проедьте на машине, чтобы плотность раствора сравнялась. Есть еще один совет: доливайте дистиллированную воду в аккумулятор при работающем двигателе. Это обеспечит ее перемешивание с кислотой.
Ускорение электролиза способствует уплотнению активной массы. Этой “болезнью” страдают отрицательные пластины, активная масса которых во время эксплуатации постепенно уплотняется, а ее пористость уменьшается. Доступ электролита внутрь отрицательных пластин затрудняется, что снижает ёмкость батареи. К тому же уплотнение активной массы может сопровождаться образованием трещин и отслаиванием.
Доступ электролита внутрь отрицательных пластин затрудняется, что снижает ёмкость батареи. К тому же уплотнение активной массы может сопровождаться образованием трещин и отслаиванием.
Пластины коробятся при увеличении силы зарядного тока, при коротком замыкании, понижении уровня электролита, частом и продолжительном включении стартера, когда батарея нагружается разрядным током большой силы. Чаще короблению подвержены положительные пластины, при этом в их активной массе образуются трещины, и она (активная масса) начинает выпадать из решеток.
Причиной выпадения активной массы из решеток пластин может стать длительная перезарядка, плохое крепление пластин, вибрация и т.д. Осыпающийся активный слой в конце-концов замыкает пластины, сокращает мощность и срок службы. В современных аккумуляторах пластины помещаются в конверт-сепараторы; осадок выпадает, но короткого замыкания удается избежать.
Летом вентиляционные отверстия забиваются пылью. Чтобы батарея не лопнула и не взорвалась следите за чистотой аккумулятора. Пробки заливных отверстий должны быть плотно закрыты.
Пробки заливных отверстий должны быть плотно закрыты.
Как сохранить свой аккумулятор летом?
Во-первых, следите за уровнем электролита и регулярно доливайте дистиллированную воду. Во-вторых, не оставляйте батарею незаряженной. В-третьих, следите за чистотой корпуса. В-четвертых, следите за состоянием электрической системы автомобиля. Неисправный стартер и генератор совершенно незаметно “подготовят” батарею к зиме и с первыми морозами она откажет.
Если вы планируете заменить аккумулятор, лучше не ждать до осени. В сезон выбор значительно меньше, цены выше, а желающих больше. В любом случае потребуется помощь подготовленного продавца-консультанта. Летом он сможет больше уделить вам времени.
10. Вопросы безопасности
Помните, что опасность возгорания кислорода и водорода, выделяющихся во время зарядки (а также после ее завершения), вполне реальна.
Хотя большинство серьезных производителей оборудуют крышки аккумуляторов ограничителями пламени, призванными предотвратить его попадание внутрь аккумулятора, подобная вероятность по-прежнему сохраняется.
Помните также, что искра возникает не только при отсоединении клеммы. Статического электричества от синтетической одежды может оказаться достаточно, чтобы вызвать взрыв.
Взрыв аккумулятора можно сравнить по мощности с выстрелом из ружья калибра 12мм. Результат представляет собой жуткое зрелище, и происходит это чаще, чем вы можете себе представить. При том, что взрыв, вероятно, не будет смертельным, он может серьезно травмировать вас, особенно лицо, так как осколки пластика разлетаются во все стороны. Поэтому всегда следует быть в защитных очках.
Если вдруг позарез понадобилось отсоединить аккумулятор на машине с работающим мотором (лучше, конечно, не подвергать свой автомобиль таким испытаниям), прежде надо включить как можно больше потребителей электроэнергии: печку, фары, противотуманки, «дворники». Если этого не сделать, то может сгореть регулятор напряжения, а следом откажет электрооборудование и в том числе — системы управления двигателем. А для начала загляните в инструкции: позволяет ли она вообще производить такую операцию. Ведь на автомобилях некоторых марок, напичканных современной аппаратурой, любое отключение аккумулятора выводит из строя сложные электронные системы.
Ведь на автомобилях некоторых марок, напичканных современной аппаратурой, любое отключение аккумулятора выводит из строя сложные электронные системы.
11. Хранение аккумуляторной батареи
1.снимите аккумулятор с машины (оставьте на машине со снятыми клеммами), очистите от грязи, полностью зарядите.
2.при отсутствии возможности подзарядки во время хранения АКБ можно рекомендовать следующий способ. Электролит в аккумуляторе необходимо заменить 5-процентным раствором борной кислоты. Перед заменой электролита АКБ полностью заряжают, а затем сливают электролит в течение 15 минут. Затем ее сразу же промывают дважды дистиллированной водой, выдерживая воду по 20 минут. После промывки наливают раствор борной кислоты, заворачивают пробки с открытыми вентиляционными отверстиями, вытирают батарею и ставят на хранение. Саморазряд аккумуляторов с раствором борной кислоты практически отсутствует.
Справка
Для приготовления 5-процентного раствора борной кислоты необходимо в 1 литре дистиллированной воды, нагретой до 50. ..60°С, растворить 50г борной кислоты. Раствор заливают в аккумуляторы при температуре 20…30°С.
..60°С, растворить 50г борной кислоты. Раствор заливают в аккумуляторы при температуре 20…30°С.
Хранить батарею надо при температуре не ниже 0°С, поскольку заливаемый 5-процентный раствор борной кислоты может замерзнуть. А для ввода такой батареи в действие из нее выливают раствор борной кислоты в течение 15…20 минут и сразу же заливают сернокислый электролит плотностью 1.38…1.40 г/см3 для нашей зоны. После 40-минутной пропитки пластин электролитом АКБ можно устанавливать на автомобиль, если плотность электролита не уменьшилась ниже 1.24…1.25 г/см3. Если она стала ниже, следует откорректировать плотность отбором слабого раствора и добавлением электролита плотностью 1.40 г/см
12. Приложения
12.1. Реанимация аккумулятора
Реанимация аккумулятора. Старый фирменный аккумулятор может послужить еще, если его правильно восстановить! Итак, начнём. Имеем на руках убитый или почти убитый аккумулятор.
Нам понадобятся некоторые материалы и инструменты:
1) Свежий электролит (номинальной + желательно повышенной плотности)
2) Дистиллированная вода.
3) Измеритель плотности электролита (ареометр). Например ареометр производства НПП «Орион CПб»
4) Зарядное устройство, способное обеспечить малые (0.05-0.4А) токи зарядки.
5) Маленькая клизма (простите, надо!) и пипетка для наливных целей.
6) Нагрузочная вилка. НПП «Орион СПб» производит 4 модели: от простых и дешевых НВ-01, НВ-02, до профессиональных НВ-03, НВ-04.
Для начала определимся с возможными неисправностями:
1) Засульфатированность пластин — ёмкость аккумулятора падает почти до нуля.
2) Разрушение угольных пластин — при зарядке электролит становится черным.
3) Замыкание пластин — электролит в одной из секций аккумулятора выкипает, секция греется. (Тяжелый случай, но иногда небезнадежный)
4) Перемёрзший аккумулятор — распухшие бока, электролит при заряде сразу вскипает (многочисленные замыкания пластин) — тут уж ничем не помочь, аминь, упокой Господь его душу!
Начнем с конца списка. (п.3) При замыкании пластин ни в коем случае не пытайтесь его заряжать! Начинаем промывку дистиллированной водой. Не бойтесь переворачивать и трясти аккумулятор, хуже уже не будет. Промывайте его до тех пор, пока не перестанет вымываться угольная крошка (надеюсь, этот момент наступит, иначе прекратите этот мазохизм). При промывке часто замыкание пластин устраняется, и мы переходим от пункта (3) к пункту (2). После промывки и вытряхивания всякого мусора из недр аккумулятора приступаем к пункту (1), а именно к устранению отложений солей на пластинах аккумулятора. Следуйте инструкциям к присадке. Мой опыт может отличаться от того, что вы прочтёте в инструкции. Далее я делаю так:
Не бойтесь переворачивать и трясти аккумулятор, хуже уже не будет. Промывайте его до тех пор, пока не перестанет вымываться угольная крошка (надеюсь, этот момент наступит, иначе прекратите этот мазохизм). При промывке часто замыкание пластин устраняется, и мы переходим от пункта (3) к пункту (2). После промывки и вытряхивания всякого мусора из недр аккумулятора приступаем к пункту (1), а именно к устранению отложений солей на пластинах аккумулятора. Следуйте инструкциям к присадке. Мой опыт может отличаться от того, что вы прочтёте в инструкции. Далее я делаю так:
1) Заливаем аккумулятор электролитом номинальной плотности (1.28 г/см3).
2) Добавляем присадку, исходя из объёма аккумулятора (см. инструкцию)
3) Даём электролиту выдавить воздух из секций, а присадке — раствориться в течении 48 часов (!), при необходимости доливаем электролит до номинального уровня. Кстати, присадку можно растворить в электролите до заливки в аккумулятор, если, конечно, она хорошо растворяется.
4) Подключаем зарядное устройство (не забудьте снять пробки!). НО МЫ НЕ БУДЕМ ЕГО ЗАРЯЖАТЬ! НЕ СЕЙЧАС! Сначала мы будем гонять его по циклу «зарядка-разрядка», иначе «тренировка», то есть заряжать и разряжать его, пока не восстановится нормальная ёмкость. Выставляем ток зарядки в районе 0.1- 0.2 А и следим за напряжением на клеммах. Не давайте электролиту кипеть или нагреться! Если необходимо, уменьшите зарядный ток, пузырьки газа и перегрев разрушают аккумулятор! Заряжайте, пока напряжение на клеммах аккумулятора не достигнет 2.3 — 2.4В на каждую секцию, т.е. для 12-вольтового аккумулятора — 13.8-14.4 В.
5) Уменьшаем зарядный ток вдвое и продолжаем зарядку. Зарядку аккумулятора прекращаем, если в течении 2 часов плотность электролита и напряжение на клеммах остаются неизменными.
6) Доводим плотность до номинальной доливкой электролита повышенной плотности (1.4) или дистиллированной воды.
7) Разряжаем аккумулятор через лампочку током примерно в 0. 5А до падения напряжения на клеммах до 1.7В на элемент. Для 12-вольтового аккумулятора эта величина составит 10.2В, для 6-вольтового 5.1 соответственно. Из имеющихся величин тока разряда и времени разряда вычисляем ёмкость нашего аккумулятора. Если она ниже номинальной (4 ампер-часа), то:
5А до падения напряжения на клеммах до 1.7В на элемент. Для 12-вольтового аккумулятора эта величина составит 10.2В, для 6-вольтового 5.1 соответственно. Из имеющихся величин тока разряда и времени разряда вычисляем ёмкость нашего аккумулятора. Если она ниже номинальной (4 ампер-часа), то:
Повторяем цикл заряда с начала до тех пор, пока ёмкость аккумулятора не приблизится к номинальной.
9) Добавляем в электролит ещё немного присадки и закрываем отверстия аккумулятора. ВСЁ!!! Мы имеем на руках рабочий аккумулятор, который, иногда способен проработать дольше китайского!
Дальше обращаемся с аккумулятором, как положено.
12.2. Ещё несколько способов, основанных на использовании электрического тока.
Способ первый — простой. Электролит заменить дистиллированной водой и зарядить аккумулятор или батарею очень небольшим (примерно 0.01 ёмкости) током. При этом в банках степень сульфатации снижается и образуется электролит, который заменять не нужно. После двух часов зарядки ее прекращают на такое же время. А затем снова повторяют.
А затем снова повторяют.
Доказано, что после одного-трех таких циклов степень сульфатации резко снижается.
Второй способ — наиболее трудоемкий, но в безвыходном положении его тоже можно применить. Он химический, включает следующие операции: заряд батареи в течение 2…3 часов, слив электролита из банок, двух-трехкратная их промывка дистиллированной водой, заправка 2.5-процентным (25 г на 1 л) раствором питьевой соды и выдержка в течение 2…3 часов, слив раствора, заправка 2…3-процентным раствором повареной соли, заряд батареи в течение 1ч, слив раствора, промывка 4-процентным раствором питьевой соды, полный (из расчета 150-процентной ёмкости) заряд батареи, третья промывка банок, заправка их электролитом, полный (150-процентной ёмкости) заряд батареи.
Добавление соли в лед в холодильнике
Почему люди иногда добавляют соль в лед в холодильнике для напитков или пива? Это простой вопрос. В Интернете есть множество статей и видео, но я не смог найти исчерпывающего объяснения того, почему это работает.
Некоторые основы
Важно сначала понять, что означают точка плавления и точка замерзания .
Температура плавления является свойством твердых тел. Температура плавления — это просто температура, при которой твердое вещество превращается в жидкость.Например, температура плавления обычного льда составляет 0°C при стандартном давлении.
Температура замерзания является свойством жидкостей. Точка замерзания — это просто температура, при которой жидкость превращается в твердое тело. Таким образом, температура замерзания обычной пресной воды равна 0°С.
Значения точек плавления и замерзания одинаковы (т.е. обе точки равны 0°C для воды).
Как видите, точка плавления и точка замерзания являются своего рода «зеркалами» друг друга.
О температуре замерзания твердого тела говорить не имеет смысла (так как оно уже затвердело).
Что делает соль?
Когда в воду добавляют соль, она снижает температуру замерзания. Другими словами, вода должна быть охлаждена до температуры ниже 0°C (например, -2°C), чтобы превратиться в лед. Другой способ сказать то же самое состоит в том, что соль позволяет воде существовать в виде жидкости при температуре ниже 0°C. Это важная часть, относящаяся к охладителям пива. Мы вернемся к этому позже.
Другими словами, вода должна быть охлаждена до температуры ниже 0°C (например, -2°C), чтобы превратиться в лед. Другой способ сказать то же самое состоит в том, что соль позволяет воде существовать в виде жидкости при температуре ниже 0°C. Это важная часть, относящаяся к охладителям пива. Мы вернемся к этому позже.
Для полноты картины давайте посмотрим на это с точки зрения точки плавления.Когда соль добавляется в лед, она снижает температуру плавления. Другими словами, лед начинает таять при температуре ниже 0°C. Вот почему зимой в лед на дорогах добавляют соль. Это заставляет лед, который в противном случае оставался бы твердым при минусовых температурах, превращался в воду. Обратите внимание, что температура воды не изменилась. Он все еще находится при минусовой температуре, но, как упоминалось выше, соль позволяет ему оставаться в жидком состоянии при более низкой температуре.Не думайте, что только потому, что соленый лед стал водой, температура поднялась.
Как это относится к охладителям пива?
Двумя способами: быстро охладить пиво и сохранить пиво холодным.
Быстрое охлаждение пива
Важной частью быстрого охлаждения пива является максимальное увеличение площади поверхности банки/бутылки, контактирующей с охлаждающим агентом, будь то лед, вода или холодный воздух.
Соленая вода позволяет очень быстро охладить теплое пиво — намного быстрее, чем морозильник [1].Налейте холодную воду, лед и соль в кулер, чтобы создать ванну с солью, водой и льдом. Почему это работает? Лед будет иметь температуру намного ниже нуля, обычно -18°C для бытового морозильника [2]. Лед охладит воду, а соль позволит температуре воды упасть ниже 0°C. После этого пиво будет полностью погружено в воду с температурой ниже нуля, что максимально увеличит площадь соприкосновения с поверхностью.
Без соли вода останется при температуре немного выше 0°C, даже если в ней плавают кубики льда -18°C.Вода все равно станет довольно холодной и сослужит хорошую службу, но не такой холодной, как соленая вода.
Если вы положите в холодильник только лед, то меньшая часть поверхности пива будет соприкасаться с охлаждающим агентом (льдом), поскольку кубики льда имеют неправильную форму. Он не охладит пиво так быстро, как соленая вода.
Сохранение пива холодным
Если ваша цель — сохранить пиво холодным в течение длительного времени (например, если вы отправляетесь в поход или на пикник), все равно рекомендуется добавить немного воды и соли в лед, потому что это сначала сделает ваше пиво более холодным, что означает они дольше останутся холодными.Соль также заставит лед растаять, но полученная вода все равно будет очень холодной. Удельная теплоемкость воды в два раза выше, чем у льда [3], а это означает, что теоретически минусовая вода будет оставаться холоднее, чем обычный лед. Вы можете возразить, что начальная температура льда намного ниже (-18°C), чем минусовая температура воды (которая может быть всего на несколько градусов ниже 0°C). Так что это своего рода компромисс. Кроме того, добавление соли в воду снижает ее теплоемкость, но ненамного [4].
Кроме того, добавление соли в воду снижает ее теплоемкость, но ненамного [4].
Примечание: вам нужно много соли (горсти), чтобы все вышеперечисленное работало.Поваренная соль подойдет.
Ссылки
- http://youtu.be/k3PvQXlxvZY
- http://www.inspection.gc.ca/food/consumer-centre/food-safety-tips/food-handling/kitchen/eng/132916
68/1329169127007 - http://en.wikipedia.org/wiki/Properties_of_water#Water.2C_ice_and_vapor
- http://www.kayelaby.npl.co.uk/general_physics/2_7/2_7_9.html
Нравится:
Нравится Загрузка…
Как сделать соляной раствор для дорог — Библиотека соли
Красивая сцена снегопада делает нас всех счастливыми.Успокаивающий вид белого цвета на улицах несет в себе настоящий дух зимы. Но эта воодушевляющая картина также означает, что тротуары и дороги за ночь покроются льдом, и это повлияет на всю транспортную систему. Но раствор под названием соляной раствор предотвращает замерзание снега. Он широко используется, и вы также можете узнать , как приготовить соляной раствор для дорог .
Он широко используется, и вы также можете узнать , как приготовить соляной раствор для дорог .
Вы также можете прочитать нашу статью «Как быстрее растопить снег вокруг дома», чтобы узнать, как очистить дом от снега и льда.
Почему дороги посыпают солью, когда идет снег?
Если к другому веществу добавить вещество, имеющее более низкую температуру замерзания, температура замерзания смеси будет выше, чем у первого вещества, но ниже, чем у второго вещества. Соль, брошенная на обледенелые дороги, снижает температуру плавления льда. Таким образом, лед начинает таять при температуре, при которой он обычно был бы твердым. И снег не замерзший, он не замерзнет при нормальной температуре.
Соль на самом деле не плавит лед, но снижает температуру плавления льда. Например, рассмотрим день, когда температура воздуха составляет -3 °C/27 °F. Поскольку температура плавления/замерзания чистой воды составляет 0 °C/32 °F, вода на открытом воздухе в такой день замерзнет.
Однако один из основных законов химии гласит, что температура замерзания жидкостей с примесями, смешанными с различными веществами, будет снижаться. Целью посыпания дорог солью является использование этой ситуации.
Вещество, используемое для снижения температуры таяния льда или другой жидкости, не обязательно должно быть солью. Например, того же результата можно добиться, используя сахар вместо соли.
Другим фактором, определяющим температуру плавления, является давление. Когда давление на твердое тело увеличивается, температура плавления снижается. По этой причине лед на дорогах тает в холодные зимние дни, когда большегрузные автомобили проезжают по этому льду.
Итак, вы узнали, как соль помогает растопить лед, и как Koyuncu Salt, производитель соли мирового класса, мы углубимся в эту тему и подготовим полезное руководство.
Что такое солевой раствор?
Соляная рапа представляет собой раствор соли и воды. Этот раствор имеет точку замерзания ниже, чем у чистой воды, и является полезным инструментом для уменьшения прилипания снега и льда к дорожному покрытию. В дополнение к рассолу, приготовленному с хлоридом натрия, некоторые рассолы также могут быть приготовлены с хлоридом кальция или хлоридом магния. Пониженная температура замерзания рассола является функцией упомянутых выше веществ.
В дополнение к рассолу, приготовленному с хлоридом натрия, некоторые рассолы также могут быть приготовлены с хлоридом кальция или хлоридом магния. Пониженная температура замерзания рассола является функцией упомянутых выше веществ.
Почему солевой раствор важен?
Каменная соль — это просто кристаллы хлорида натрия.Пока он не перейдет в раствор, образующий рассол, он не препятствует замерзанию снега и покрытию льдом поверхностей. Посыпание дорог солью зимой производится для того, чтобы образовалась рассол на дорожном покрытии. Соль нуждается в воде, чтобы создать рассол. Каменная соль не снижает температуру замерзания поверхности дорожного покрытия до тех пор, пока она не превратится в рассол.
Каменная соль обычно предварительно смачивается перед нанесением на поверхность. В рассоле действительно много воды.Например, раствор хлорида натрия обычно содержит 23,3% хлорида натрия при его применении. Это означает, что это 76,7% воды.
Когда снег начинает таять, рассол начинает разбавляться, что требует добавления веществ для поддержания оптимальной формулы. Так как именно соль предотвращает замерзание воды, а также способствует ускорению таяния льда, крайне важно, чтобы дороги и тротуары регулярно покрывались солевым раствором.
Так как именно соль предотвращает замерзание воды, а также способствует ускорению таяния льда, крайне важно, чтобы дороги и тротуары регулярно покрывались солевым раствором.
Как приготовить соляной раствор для дорог
Если вам интересно как сделать рассол для дорог , вот ответы.Помимо простоты смешивания, самодельный солевой раствор является более экологичной альтернативой традиционному применению каменной соли. Его можно хранить в бутылках и распылять для мелкомасштабной уборки снега и льда на проезжей части и тротуарах, а большое количество соляной смеси можно использовать на улицах и дорогах.
Вот несколько формул, которые вы можете выбрать в зависимости от того, какие ингредиенты наиболее доступны для вас!
Рассол домашнего приготовления 1
Ингредиенты
· 2 ведра
· Древесная зола
· Белый уксус
· Распылитель
· Вода
1. Положите 2 стакана древесной золы в ведро, содержащее галлон/3,8 литра воды, и хорошо перемешайте. Оставьте эту смесь на ночь.
Положите 2 стакана древесной золы в ведро, содержащее галлон/3,8 литра воды, и хорошо перемешайте. Оставьте эту смесь на ночь.
2. Через ночь очистите раствор от кусочков дерева или древесного угля, которые не растворились в воде.
3. Вылейте раствор в отдельное ведро, но избегайте остатка на дне первого ведра. Зола обеспечивает нас калием и натрием, которые нам нужны для борьбы с обледенением.
4. Добавьте в раствор белый уксус.Он будет смешиваться с натрием и калием, образуя ацетат натрия и ацетат калия.
5. Налейте рассол в распылитель или емкость большего размера и распылите его в любом месте до того, как пойдет снег.
Домашний рассол 2
Ингредиенты
· Горячая вода
· Соль
· Распылитель
· Ведро
1. Насыпьте в ведро 24–32 унции/галлон или 680–907 г/3,8 литра соли.
2. Налейте в ведро столько горячей воды, сколько необходимо, в зависимости от того, в какую емкость вы будете наливать рассол. Причиной использования горячей воды является более легкое растворение соли.
Причиной использования горячей воды является более легкое растворение соли.
3. Перемешивайте рассол до полного растворения соли.
4. Налейте рассол в распылитель или емкость большего размера и распыляйте его в любом месте до того, как пойдет снег.
Рассол домашнего приготовления 3
Ингредиенты
· Распылитель
· Соль
· Теплая вода
· Патока или сок сахарной свеклы
1.Сделайте соляной раствор, используя 22% соли и 77% воды.
2. Приготовьте раствор, используя 20% патоки или сока сахарной свеклы на 80% рассола.
3. Смешивайте до полного растворения.
4. Налейте рассол в распылитель или емкость большего размера и распыляйте его в любом месте до того, как пойдет снег.
Меласса или сок сахарной свеклы обеспечивают лучшее прилипание к поверхностям, так как препятствуют легкому рассеиванию соли.
Соль и лед
В нашей части мира температура зимой достаточно низкая для образования снега и льда.Это может сделать вождение и ходьбу опасными, поскольку дороги и тротуары становятся скользкими. В западной части Нью-Йорка каменная соль часто используется для растапливания обледенелых дорог. Взаимодействие соли и льда интересно исследовать.
Положите два кубика льда в два стакана. На один кубик льда положите чайную ложку поваренной соли. Какой кубик льда тает быстрее, тот, что с солью, или тот, что без соли? Почему это происходит?
Кубик льда без соли тает, потому что воздух вокруг него теплее 32 градусов по Фаренгейту.Солёный кубик тает быстрее. Когда вы добавляете соль, она растворяется в воде кубика льда. Соленая вода замерзает при более низкой температуре, чем 32 градуса по Фаренгейту, при которой замерзает пресная вода. Разница между температурой воздуха и точкой замерзания соленой воды больше, чем разница между температурой воздуха и точкой замерзания пресной воды. Это заставляет лед с солью таять быстрее.
Соленая вода замерзает при более низкой температуре, чем 32 градуса по Фаренгейту, при которой замерзает пресная вода. Разница между температурой воздуха и точкой замерзания соленой воды больше, чем разница между температурой воздуха и точкой замерзания пресной воды. Это заставляет лед с солью таять быстрее.
Попробуйте положить лед в стакан с холодной водой. Оставьте его там на 10 минут или около того.Какая температура воды? Проверяйте температуру каждые несколько минут. Становится ли холоднее?
Далее добавьте в воду столовую ложку поваренной соли. Смешать лед, соль и воду. Температура меняется? Продолжайте помешивать. Какую температуру можно получить?
Вот почему. Соль растворяется в воде. Пресная вода замерзает при температуре 32 градуса по Фаренгейту (0 градусов по Цельсию). Соленая вода замерзает при более низких температурах, в зависимости от того, сколько соли в воде. Когда лед превращается в воду, для перехода из твердого состояния в жидкое требуется тепло. Это похоже на то, как вода переходит из жидкого состояния в газообразное, например, когда испаряющийся пот охлаждает вашу кожу. Когда лед тает, тепло отбирается от льда и воды вокруг него. Оба становятся холоднее. Насколько холодными могут быть лед, вода и соль? Когда температурная шкала Фаренгейта была впервые создана, 0 градусов по Фаренгейту были самой низкой температурой, которую можно было получить с помощью соли, воды и льда.
Это похоже на то, как вода переходит из жидкого состояния в газообразное, например, когда испаряющийся пот охлаждает вашу кожу. Когда лед тает, тепло отбирается от льда и воды вокруг него. Оба становятся холоднее. Насколько холодными могут быть лед, вода и соль? Когда температурная шкала Фаренгейта была впервые создана, 0 градусов по Фаренгейту были самой низкой температурой, которую можно было получить с помощью соли, воды и льда.
Чтобы узнать, как приготовить мороженое в пластиковом пакете, нажмите здесь. Это одна из нескольких ссылок на странице о том, как использовать соль для растапливания льда, на сайте How Stuff Works.
Как действует соль и обзор химикатов против обледенения
.
| Как работают антиобледенители? |
|---|
Противообледенители снижают температуру замерзания воды. При выборе антиобледенителя необходимо учитывать множество факторов, одним из наиболее важных факторов является температура дорожного покрытия и тенденция изменения температуры дорожного покрытия. Например, каменная соль может таять до -6 o F при температуре дорожного покрытия, но чем холоднее дорожное покрытие, тем медленнее она работает. Лучше всего избегать использования сухой каменной соли при температуре дорожного покрытия ниже 15 90 239 o 90 240 F, так как это слишком медленно.Наиболее распространенный подход к ускорению процессов таяния — добавление жидкого антиобледенителя к гранулированному продукту или использование обычных жидкостей (DLA — Direct Liquid Application). Жидкости действуют намного быстрее, чем гранулированные продукты. Тип и градация вашего гранулированного продукта также будут влиять на скорость плавления. Если у вас часто остается соль на сухом асфальте после схода снега, пришло время пересмотреть свои стратегии. Одним из простых шагов является посещение обучающих курсов по умному солению, где вы узнаете больше о выборе антиобледенителя и нормах применения.Ссылка на умный календарь тренировок по засолке. Сравнение различных антиобледенителей см. Например, каменная соль может таять до -6 o F при температуре дорожного покрытия, но чем холоднее дорожное покрытие, тем медленнее она работает. Лучше всего избегать использования сухой каменной соли при температуре дорожного покрытия ниже 15 90 239 o 90 240 F, так как это слишком медленно.Наиболее распространенный подход к ускорению процессов таяния — добавление жидкого антиобледенителя к гранулированному продукту или использование обычных жидкостей (DLA — Direct Liquid Application). Жидкости действуют намного быстрее, чем гранулированные продукты. Тип и градация вашего гранулированного продукта также будут влиять на скорость плавления. Если у вас часто остается соль на сухом асфальте после схода снега, пришло время пересмотреть свои стратегии. Одним из простых шагов является посещение обучающих курсов по умному солению, где вы узнаете больше о выборе антиобледенителя и нормах применения.Ссылка на умный календарь тренировок по засолке. Сравнение различных антиобледенителей см. в этой таблице в этой таблице |
Зимние погодные условия в Миннесоте могут привести к обледенению дорог и пешеходных дорожек, что создаст опасные условия для водителей и пешеходов. Для борьбы с этой ситуацией используются антиобледенители. Антиобледенитель — это вещество, которое плавит или предотвращает образование льда, снижая температуру замерзания воды и предотвращая сцепление между льдом и мощеными поверхностями. Исследование, проведенное Университетом Маркетта, показало, что обработка дорог солью снижает количество несчастных случаев на 88 процентов и травм на 85 процентов (Kuemmel and Hanbali, 1992).
Несмотря на то, что антиобледенители способны значительно повысить безопасность дорог и пешеходных дорожек, они также могут оказывать негативное воздействие на окружающую среду и окружающую инфраструктуру. После нанесения антиобледенители перемещаются с талыми водами в наши поверхностные и грунтовые воды. Кроме того, некоторые антиобледенители вызывают коррозию и негативно воздействуют на почву, растительность и инфраструктуру. Интегрируя научные принципы в зимнее обслуживание, мы можем сократить использование антиобледенителей, не снижая при этом безопасность. Несмотря на многие негативные последствия, преимущества антиобледенителей для общественной безопасности гарантируют, что они будут использоваться долгие годы.
Интегрируя научные принципы в зимнее обслуживание, мы можем сократить использование антиобледенителей, не снижая при этом безопасность. Несмотря на многие негативные последствия, преимущества антиобледенителей для общественной безопасности гарантируют, что они будут использоваться долгие годы.
Департамент транспорта штата Айова подготовил серию обучающих материалов по уходу за автомобилем в зимний период, в которую входит видео под названием «Как работают антиобледенительные химикаты».
Список химикатов, одобренных для использования в борьбе с обледенением Департаментом транспорта Миннесоты (MnDOT), можно найти здесь. Ссылка здесь для обсуждения воздействия антиобледенителей и противообледенительных добавок на окружающую среду.
Хлоридные антиобледенители
В этом разделе рассматриваются антиобледенители на основе хлоридов: хлорид натрия (NaCl), хлорид магния (MgCl2) и хлорид кальция (CaCl2).Как правило, антиобледенители на основе хлоридов являются наименее дорогими и наиболее часто используемыми антиобледенителями на рынке.
- Хлорид натрия . Хлорид натрия является наиболее распространенным антиобледенителем, используемым в Миннесоте и США (Sleeper, 2013). По оценкам Центра водных ресурсов UMN, каждый сезон в Миннесоте используется 403 600 тонн дорожной соли, а в TCMA — 249 100 тонн дорожной соли (Overbo et al. 2019). Хлорид натрия (каменная соль) представляет собой гранулированный продукт. Он используется для приготовления рассола (жидкого хлорида натрия), и существует множество добавок, которые можно смешивать с рассолом для повышения его эффективности.Самая низкая практическая температура плавления сухой каменной соли составляет 15 градусов при температуре дорожного покрытия (Local Road Research Board, 2012).
- Хлорид магния . Хлорид магния можно приобрести в виде хлопьев, гранул или жидкости. Самая низкая практическая температура плавления дорожного покрытия из хлорида магния составляет -10°F. Хлорид магния часто используется в виде смеси, а не в чистом виде.

- Хлорид кальция . Хлорид кальция можно приобрести в виде хлопьев, гранул или жидкости.Его самая низкая практическая температура плавления дорожного покрытия составляет -20°F (Local Road Research Board, 2012). Хлорид кальция часто используется в виде смеси, а не в чистом виде.
- Сложные хлоридные минералы : это продукты, добываемые из земли, которые не являются чистой каменной солью, а содержат множество других минералов, смешанных с ними. В целом было показано, что они повышают эффективность при более низких температурах дорожного покрытия по сравнению с камнем. соль. Хлорсодержащие жидкие сельскохозяйственные побочные продукты и твердые комплексные хлоридно-минеральные продукты.
Антиобледенители, не содержащие хлорида
Существует несколько категорий не содержащих хлоридов антиобледенителей (ацетаты, формиаты, гликоли, сукцинаты и мочевина). Противообледенительные средства, не содержащие хлоридов, используются реже, чем средства, основанные на хлоридах, на дорогах, парковках, тротуарах и тропах из-за стоимости и доступности. В аэропортах почти полностью используются антиобледенители, не содержащие хлора. Системы распыления на мостах, парковочные пандусы и зоны с низким уровнем коррозии часто используют продукты, не содержащие хлоридов.
В аэропортах почти полностью используются антиобледенители, не содержащие хлора. Системы распыления на мостах, парковочные пандусы и зоны с низким уровнем коррозии часто используют продукты, не содержащие хлоридов.
Ацетаты для защиты от обледенения
В Миннесоте ацетаты чаще используются при зимнем обслуживании дорог, чем другие антиобледенители, не содержащие хлоридов.В семейство ацетатов входят ацетат натрия, ацетат кальция, магния и ацетат калия (КАС).
- Ацетат кальция-магния (CMA). CMA можно приобрести в виде порошка, кристаллов, гранул или жидкости. CMA имеет самую низкую практическую температуру плавления дорожного покрытия 20 ° F (Местный совет по исследованиям дорог, 2012 г.).
- Ацетат калия (KAc). KAc обычно приобретается в жидком виде, и его самая низкая практическая температура плавления дорожного покрытия составляет -15°F (Местный совет по исследованиям дорог, 2012 г.).
Ацетат калия получил наибольшее внимание при строительстве дорог. Он используется в автоматизированных системах защиты от обледенения мостов, а Департамент транспорта Миннесоты (MnDOT) District 1 использует маршрут только KAC в районе Дулута. Из-за эффективности в диапазоне низких температур и более широкого использования и успеха этого продукта проводятся исследования, чтобы лучше понять побочные эффекты KAC на окружающую среду и инфраструктуру (MnDOT и UMN St. Anthony Falls Laboratory; Xie et al., 2017.
Он используется в автоматизированных системах защиты от обледенения мостов, а Департамент транспорта Миннесоты (MnDOT) District 1 использует маршрут только KAC в районе Дулута. Из-за эффективности в диапазоне низких температур и более широкого использования и успеха этого продукта проводятся исследования, чтобы лучше понять побочные эффекты KAC на окружающую среду и инфраструктуру (MnDOT и UMN St. Anthony Falls Laboratory; Xie et al., 2017.
Аэропорты больше инвестируют в использование антиобледенителей без хлора, чем в индустрию обслуживания дорог/парковок/тротуаров, при этом ацетат калия является ведущим жидким растворителем для взлетно-посадочных полос, ацетат натрия является ведущим гранулированным антиобледенителем, а гликоли обычно используются для борьбы с обледенением самолетов. Для получения более подробной информации посетите страницу Контроль снега и льда для работы аэропорта. Обзор использования и изучение антиобледенителей, не содержащих хлоридов, см. в разделе «Использование альтернативных антиобледенителей для борьбы со снегом и льдом в полевых условиях» и «Материалы для борьбы со снегом и льдом без содержания хлоридов», 2014 г.
Преимущества ацетатов заключаются в следующем.
К недостаткам ацетатов относятся следующие.
- Реагирует с цинком и разъедает его, что может повлиять на оцинкованную сталь (Fortin, et al 2014).
- Потенциально приводит к бескислородной среде при разложении (Levelton Consultants Ltd., 2008).
- Требуется больше материала по сравнению с солью, чтобы получить сопоставимое таяние льда. По оценкам, потребуется дополнительно от 20 до 70 процентов по весу (NRC, 1991).
- Не работает так же хорошо, как антиобледенители на основе хлоридов при температуре дорожного покрытия ниже -5°C во время сильного снегопада и ледяного дождя (NRC, 1991).
Антиобледенители из отходов
Продукты потока отходов для удаления льда исторически включали хлоридные и нехлоридные соединения. Другие варианты антиобледенителя включают бесплатный или недорогой рассол для сыра, рассол или другие побочные продукты промышленности для защиты от обледенения или устранения обледенения. Однако их не следует использовать без принятия соответствующих мер.Шаги, которые необходимо предпринять перед использованием продукта потока отходов, включают, но не ограничиваются следующим [1].
Однако их не следует использовать без принятия соответствующих мер.Шаги, которые необходимо предпринять перед использованием продукта потока отходов, включают, но не ограничиваются следующим [1].
- Определить, соответствует ли химический состав каждой партии отходов
- Определите побочные эффекты этого продукта
- Определите, что с ним нужно смешивать и в каком количестве для достижения оптимальной производительности
- Получите разрешение на применение в вашем регионе
- Протестируйте его на небольшом участке и узнайте, как он работает
Дополнительную информацию см. ниже.
Противогололедные добавки
Углеводы являются добавкой к антиобледенителям и представляют собой сельскохозяйственный продукт, часто получаемый в результате ферментации зерна или переработки сахаров, таких как тростниковый или свекловичный сахар (Rubin et al., 2010). Небольшие количества углеводов иногда используются с другими антиобледенителями.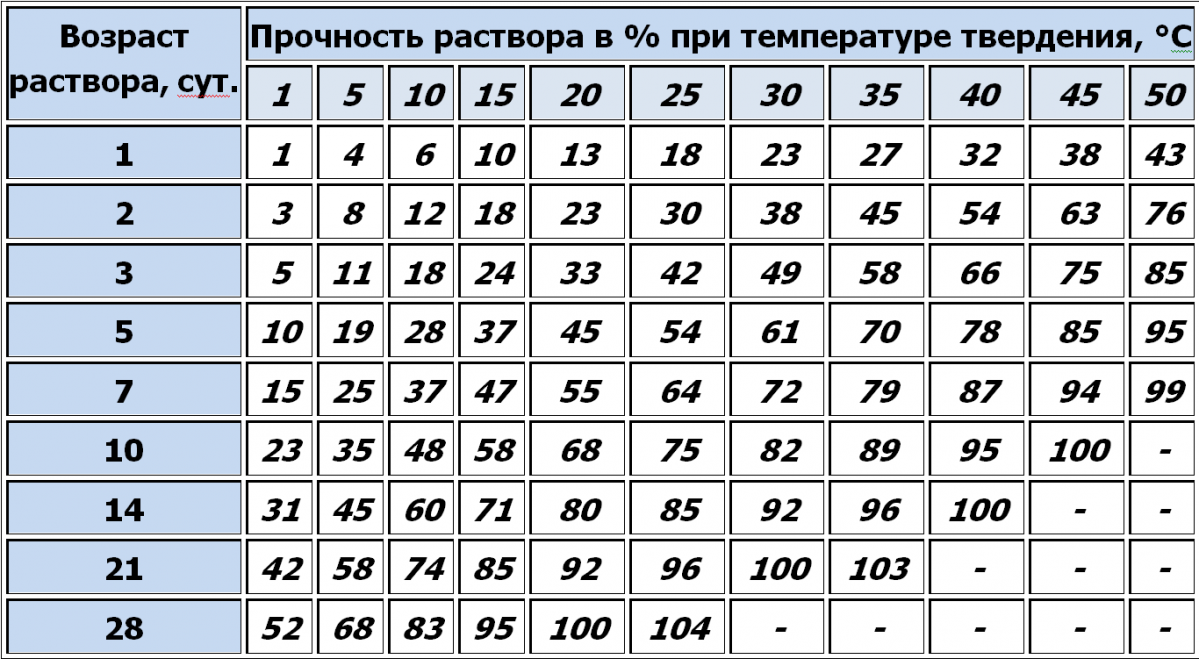
Добавление сельскохозяйственной добавки в рассол или каменную соль имеет свои плюсы и минусы. Сами по себе углеводы не способствуют таянию льда или снега. Сельскохозяйственная продукция может оказывать краткосрочное негативное воздействие на окружающую среду, включая заметное цветение водорослей или гибель рыбы.Тем не менее, смешанные с хлоридными продуктами, они могут снизить нормы применения антиобледенителей и повысить эффективность антиобледенителей в различных ситуациях. К наиболее распространенным положительным аспектам этих добавок относятся следующие (Fortin et al, 2014; Rhodan and Sanburn, 2014).
- вмешательство в образование кристаллов льда
- снижение точки замерзания рассола
- повышенное «прилипание» к поверхностям
- снижение коррозии
Информацию по этой теме см. в документе «Понимание эффективности не содержащих хлорид жидких сельскохозяйственных побочных продуктов и твердых комплексных хлоридно-минеральных продуктов» на веб-сайте ClearRoads.
Резюме
Обобщающая таблица свойств противогололедных реагентов. Адаптировано из материалов Local Road Research Board, 2012 г., Ketcham et al., 1996 г. и Levelton Consultants Ltd., 2008 г.
Ссылка на эту таблицу
| Категория | Тип | Самая низкая практическая температура плавления дорожного покрытия | Возможность коррозионного повреждения 3 | Воздействие на окружающую среду | |||||
|---|---|---|---|---|---|---|---|---|---|
| Атмосферная коррозия металлов | Бетонная матрица | Армирование бетона | Качество воды/водная жизнь | Качество воздуха | Почвы | Растительность | |||
| Антиобледенители на основе хлорида | Хлорид натрия | 15°F | Высокий; инициирует и ускоряет коррозию | Низкий/умеренный; усугубит масштабирование; низкий риск атаки пастой | Высокий: вызывает коррозию арматуры | Умеренная: чрезмерное содержание хлоридов/загрязнителей металлов; ферроцианидные добавки | Низкий: приводит к сокращению использования абразивов | Умеренный/высокий: Накопление натрия разрушает структуру почвы и снижает проницаемость и стабильность почвы; способность металлов мобилизовать | Высокий: Опрыскивание вызывает повреждение листвы; осмотический стресс повреждает корни, хлоридный токсикоз |
| Хлорид кальция | -20°F | Высокий; Инициирует и ускоряет коррозию; более высокий потенциал коррозии, связанный с гигроскопическими свойствами | Низкий/умеренный; усугубит масштабирование; низкий риск атаки пастой | Высокий: вызывает коррозию арматуры | Умеренная: чрезмерное содержание хлоридов; загрязнение тяжелыми металлами | Низкий: приводит к сокращению использования абразивов | Низкий/умеренный: улучшает структуру почвы; повышает проходимость; способность металлов мобилизовать | Высокий: Опрыскивание вызывает повреждение листвы; осмотический стресс повреждает корни, хлоридный токсикоз | |
| Хлорид магния | -10°F | Высокий; Инициирует и ускоряет коррозию; более высокий потенциал коррозии, связанный с гигроскопическими свойствами | Умеренный/высокий: усугубит масштабирование; риск порчи пасты из-за магния | Высокий: Инициирует коррозию арматуры, данные свидетельствуют о том, что MgCl2 имеет самый высокий потенциал коррозии хлоридов | Умеренная: чрезмерное содержание хлоридов; загрязнение тяжелыми металлами | Низкий: Приводит к сокращению количества абразивов | Низкий/умеренный: улучшает структуру почвы; повышает проходимость; способность металлов мобилизовать | Высокий: Опрыскивание вызывает повреждение листвы; осмотический стресс повреждает корни, хлоридный токсикоз | |
| Антиобледенители на основе ацетата | Ацетат кальция и магния | 20°F [2] | Низкий/умеренный; Возможность инициирования и ускорения коррозии из-за повышенной проводимости | Умеренный/высокий: усугубит масштабирование; риск порчи паштета из-за реакций с магнием | Низкий; вероятно мало или нет эффекта | Высокий: органическое содержание приводит к потребности в кислороде | Низкий: приводит к сокращению использования абразивов | Низкий/умеренный: улучшает структуру почвы; повышает проходимость; способность металлов мобилизовать | Низкий: Небольшой побочный эффект или его отсутствие; осмотический стресс при высоких уровнях |
| Ацетат калия | -26°F [3] | Низкий/умеренный; Возможность инициирования и ускорения коррозии из-за повышенной проводимости | [4] | Низкий; вероятно, мало или совсем не влияет [5] | Высокий: органическое содержание приводит к потребности в кислороде | Низкий: приводит к сокращению использования абразивов | |||
| Ацетат натрия | 0°F [6] | Относительная водная токсичность: высокая | |||||||
| Углеводы | Свекольный сок | нет данных | Низкий; Потенциал инициирования и ускорения коррозии из-за повышенной электропроводности моллюсков для смягчения коррозии требует дальнейшей оценки | Низкий; Вероятно, незначительный эффект или его отсутствие | Низкий; Вероятно, небольшой эффект или его отсутствие; заявления об уменьшении коррозии требуют дальнейшей оценки | Высокое содержание органических веществ, приводящее к потребности в кислороде; обогащение питательных веществ фосфором и азотом; тяжелые металлы | Низкий: приводит к сокращению использования абразива | Низкий: Вероятно, небольшой эффект или его отсутствие; доступная ограниченная информация | Низкий: Вероятно, мало или нет эффекта |
| Меласса | нет данных | ||||||||
| Кукурузный сироп | нет данных | ||||||||
Связанные страницы
Как холодно слишком холодно, чтобы мыть машину
Уход за автомобилем и его техническое обслуживание — это целое усилие само по себе. Помимо знания того, что использовать и как мыть машину, вам также нужно знать, когда мыть машину. В связи с этим частый вопрос среди автовладельцев: «Насколько холодно мыть машину?» или «Когда слишком холодно мыть машину?».
Помимо знания того, что использовать и как мыть машину, вам также нужно знать, когда мыть машину. В связи с этим частый вопрос среди автовладельцев: «Насколько холодно мыть машину?» или «Когда слишком холодно мыть машину?».
Особенно актуально с наступлением зимы и холодов.
Короткий ответ: слишком холодно для автомойки, если температура близка к нулю или замерзает. В частности, это где-то от и ниже 34 градусов по Фаренгейту.
Однако в этой статье есть и другие важные детали и советы. Итак, продолжайте читать, чтобы узнать!
Как холодно слишком холодно, чтобы мыть машину
Температура замерзания воды составляет 0 градусов по Цельсию или 32 градуса по Фаренгейту. Таким образом, если температура находится на этом уровне, вы НЕ должны мыть машину. Почему? Потому что, если вы не успеете высушить машину после мойки, она замерзнет.
В частности, петли, ручки и замки будут закрыты льдом.Поверьте, нет ничего хуже дверных косяков. Даже если у вас может возникнуть соблазн просто быстро помыть машину из шланга, лучше подождать, пока температура не поднимется.
Как правило, безопасная температура для мойки автомобиля составляет 49 градусов по Фаренгейту и выше. Однако идеальная температура составляет от 50 до 89 градусов.
Значит, зимой нельзя мыть машину? Точно нет! Это распространенная, но смертельная ошибка среди пользователей автомобилей. На самом деле очень важно, чтобы вы чистили свой автомобиль зимой, потому что в это время года ваш автомобиль может собрать много солевых смесей и отложений.Поскольку дороги обычно покрыты слоями соли, чтобы свести к минимуму случаи заноса на скользкой поверхности, отложения соли неизбежны.
К сожалению, распространенным последствием этого является солевая коррозия, то есть части вашего автомобиля разъедаются солью. Наиболее уязвимыми компонентами являются компоненты ходовой части, такие как топливная магистраль автомобиля. Если не помыть машину зимой, можно испортить ее внешний вид. В свою очередь, вам придется выложить немалые деньги на ремонт.
Итак, вместо ручной мойки в холодную погоду рассмотрите услуги автомойки.
Варианты мойки зимой:
Бесконтактные автомойки
Эти услуги упрощают мойку автомобилей. Вам просто нужно проехать и дождаться, пока вашу машину помоют. Они также достаточно доступны по цене; Вам не нужно беспокоиться об исчерпании своего кошелька!
Однако в большинстве бесконтактных автомоек используются шланги высокого давления, которые потенциально могут протолкнуть соль глубже в любые закоулки. Они часто используют агрессивные моющие средства и химикаты, которые могут быть несовместимы с краской и конструкцией поверхностей вашего автомобиля.
Но, в то же время, можно утверждать, что шланги высокого давления лучше справляются со смывом скрытых загрязнений в труднодоступных местах.
Если вы решились на бесконтактную мойку автомобилей, ищите те, которые оснащены высокопроизводительными воздуходувками или сушилками. Это значительно ускоряет процесс сушки и сводит к минимуму вероятность замерзания воды внутри или на поверхности автомобиля.
Туннельные мойки Soft Touch
Как следует из названия, в этих моющих службах используются мягкие пенопластовые и войлочные тряпки для чистки автомобилей и очистки.Они эффективно удаляют стойкие пятна, включая органические вещества, такие как птичий помет, брызги насекомых и т. д. Они также хорошо удаляют труднодоступные поверхности, такие как пороги, задняя часть и передний номерной знак. С этими туннельными моющими средствами вы обязательно получите тщательную уборку.
Однако они более склонны к истиранию и царапинам, которые не только некрасивы, но и повреждают восковое покрытие. Они не подходят для определенных типов транспортных средств, например двухколесных грузовиков.
Если вы выберете этот вариант, убедитесь, что вы остановились на варианте с хорошей репутацией.Дешевые услуги могут не предлагать современное оборудование, которое приносит больше вреда, чем пользы. Кроме того, выберите один с прочными воздуходувками и осушителями, чтобы обеспечить процесс сушки и избежать возможности замерзания воды в любом месте вашего автомобиля.
Посмотрите это видео, если хотите более подробное сравнение между двумя вышеуказанными вариантами!
Другие варианты для рассмотрения
Если вы не являетесь поклонником услуг по мойке автомобилей, вы можете попробовать следующие обходные пути для ручной мойки автомобилей.
1. Помойте машину в отапливаемом гараже
Чтобы свести к минимуму воздействие холода, мойте машину в отапливаемом гараже. Это предотвратит замерзание воды, которую вы используете для мытья автомобиля, и возникновение косяков. Следовательно, у вас будет больше возможностей для полной просушки автомобиля.
Это может показаться тривиальным шагом, но поверьте нам, это имеет большое значение.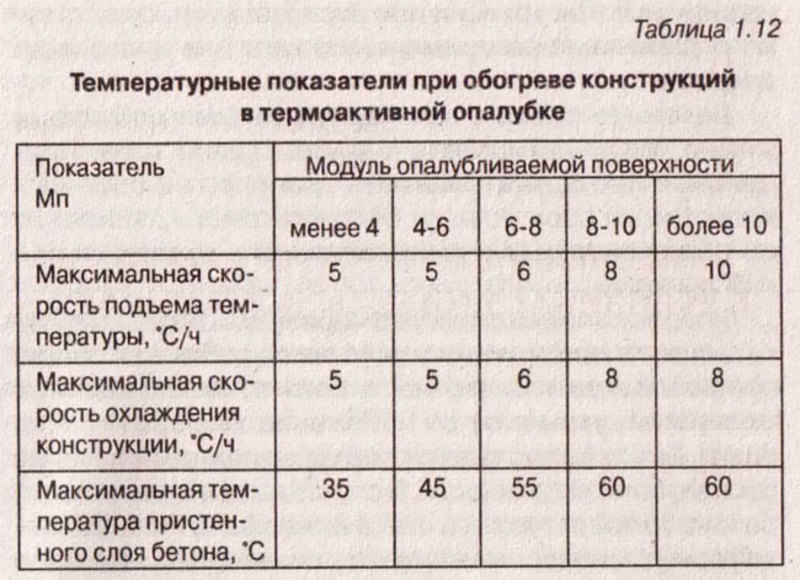
2. Запустите машину, чтобы прогреть ее до и после мойки
Если вы моете автомобиль самостоятельно, убедитесь, что вы включили двигатель и дали ему поработать не менее 30 минут, прежде чем подавать воду.Это заставит машину работать и нагревать ее, противодействуя холодным условиям, в которых вы ее моете.
После того, как вы помыли машину и прошли необходимый процесс сушки, снова включите двигатель и дайте машине поработать еще не менее 30 минут. Вырабатываемое тепло гарантирует, что остатки воды не замерзнут на нем.
Другие советы, о которых следует помнить
1. Мойте машину горячей водой
Само собой разумеется, что горячая вода противостоит холодным условиям, в которых вы моете машину.Использование горячей воды сведет к минимуму вероятность замерзания воды снаружи автомобиля. Однако важно не использовать кипящую воду, так как это может повредить качество краски вашего автомобиля.
Он также может удалить столь необходимый слой воска с поверхностей вашего автомобиля. Это особенно важно помнить, потому что вы не можете правильно наносить воск, когда температура близка к нулю. Если воск исчезнет, вы рискуете подвергнуть свой автомобиль воздействию агрессивных факторов. Опять же, это может повлечь за собой дорогостоящий ремонт в ближайшем будущем.
Это особенно важно помнить, потому что вы не можете правильно наносить воск, когда температура близка к нулю. Если воск исчезнет, вы рискуете подвергнуть свой автомобиль воздействию агрессивных факторов. Опять же, это может повлечь за собой дорогостоящий ремонт в ближайшем будущем.
2. Мойте машину во время обеда или в первой половине дня
Лучше всего мыть машину во время обеда или в начале дня, потому что именно в это время солнце светит самым ярким и излучающим тепло. Точно так же не мойте машину, когда солнце садится и на улице темно.
Вы должны записать это, чтобы запланировать подходящее время для ухода за автомобилем и технического обслуживания. Даже если это может означать несколько изменений в вашей повседневной жизни, будьте уверены, оно того стоит.
3. Распылите смазку на петли, ручки и замки
Приобретите смазку хорошего качества для распыления или нанесения тонкого слоя на дверные петли, ручки, замки, защелки и замочные скважины автомобиля. Это предотвратит попадание влаги в них и образование отложений, которые могут замерзнуть в холодную погоду.
Это предотвратит попадание влаги в них и образование отложений, которые могут замерзнуть в холодную погоду.
Вы сможете легко найти их лично в местных магазинах или виртуально в интернет-магазинах и на сайтах электронной коммерции. Если вы не знаете, с чего начать, рассмотрите возможность поиска этих надежных брендов: Permatex, DuPont и 3M.
Заключение
Таким образом, вы подошли к концу этой статьи о том, что холод слишком холоден, чтобы мыть машину. Теперь вы знаете, что мыть машину при температуре ниже нуля нельзя. Есть и другие варианты, которые вы можете использовать, и советы, которые вы можете держать в рукаве. Надеюсь, это было полезно.
Если у вас есть другие вопросы или мысли, вы можете оставить комментарий. Мы всегда ждем новостей от наших читателей. Итак, не стесняйтесь. Кроме того, не забудьте поделиться этой статьей со своими друзьями, семьей или с кем-либо, кто, по вашему мнению, оценит ее содержание.
Фермерские стада будут счастливы, пока вода в корыте говорит жидкость
Хейли Зинда
| Расширение округа Уэйн
Из-за низких температур в прошлые выходные водопроводы и водосточные желоба, вероятно, замерзли по всему штату. Если вам и вашему скоту посчастливилось иметь автоматическую поилку с нагревательным элементом, вы, возможно, не слишком сильно чувствовали холод, но для тех, у кого ее нет, я уверен, что молотки и топоры могли появиться в сараях и на полях.
Если вам и вашему скоту посчастливилось иметь автоматическую поилку с нагревательным элементом, вы, возможно, не слишком сильно чувствовали холод, но для тех, у кого ее нет, я уверен, что молотки и топоры могли появиться в сараях и на полях.
Несколько раз мне задавали вопрос: «Как предотвратить замерзание корыт без электричества?» Что ж, действительно, очень хороший вопрос.
Сначала немного о химии. Добавление соли в воду, когда вы варите лапшу, увеличивает температуру кипения воды, то есть вода горячее, чем 212 градусов. Та же концепция с соленой водой и температурой замерзания; соленая вода замерзнет при температуре ниже 32 градусов.
Теперь, когда с химией покончено, мы подошли к первому варианту — созданию поплавка для морской воды.
Катание на лошадях Давайте поиграем с управлением пастбищами
Бутылка из-под газировки и соль или закапывание корыта — несколько решений
добавьте 2 стакана соли, убедившись, что она растворяется. Закрутив крышку, поместите ее в кормушку. Он должен всплывать (если нет, вылейте немного раствора) и разрушать поверхностное натяжение воды, не замерзая.
Закрутив крышку, поместите ее в кормушку. Он должен всплывать (если нет, вылейте немного раствора) и разрушать поверхностное натяжение воды, не замерзая.
Кроме того, если кормушка начинает замерзать, стадо может научиться нажимать на бутылку, чтобы открыть жидкую воду. Вы также можете использовать футбол или баскетбол для того же эффекта.
Музыкальные братья: Дуэт Low Gap на пике популярности после выпуска первого сингла
Другой вариант — утеплить желоб комбинацией изоляции и фанеры или закопать желоб в землю.Если у вас есть возможность, вы можете соорудить фанерный ящик вокруг желоба и заполнить щели пенополистиролом, изоляцией, обернутой фольгой, или монтажной пеной.
Можно утеплить сам бак утеплителем, но фанера будет служить ветрозащитой. В то время как тактика коробки контролирует «тело» поилки, поверхность все еще открыта и может замерзнуть. Добавление фанерной крышки также может сработать, при условии, что на крышке есть пара точек доступа, через которые запас может пить.
Петли на крышке также могут быть полезными, чтобы предотвратить случайное сбивание крышки любопытным скотом или лошадьми и позволить воде замерзнуть, а также для легкого доступа для очистки резервуара, если это необходимо.
Закапывание корыта похоже на утепление тем, что земля будет теплее воздуха.
Доктор Тунес из Clarity Equine Nutrition сообщает, что просверленного отверстия диаметром 12 дюймов и глубиной в несколько футов непосредственно под кормушками было достаточно, чтобы предотвратить замерзание воды из-за геотермального тепла, исходящего от земли.
Место, место, место
Наконец, по словам наших друзей по недвижимости, «Место, место, место».
Летом под тенью дерева можно поставить поилку, но зимой в этом же месте почти никогда не будет солнца, особенно в пасмурные зимние месяцы.
Перемещение поилки в самое солнечное место в поле зимой позволит солнечному излучению нагревать поверхность поилки, поэтому найдите несколько разных мест, куда вы можете перемещать воду в течение всего года. Если ничего не помогает, вам, возможно, придется сломать и нагреть корыто или договориться с вашим верным молотком.
Если ничего не помогает, вам, возможно, придется сломать и нагреть корыто или договориться с вашим верным молотком.
Если вы в конечном итоге остановите свой выбор на обогревателе, есть несколько электрических и несколько пропановых вариантов. Варианты пропана кажутся более дорогими и предназначены для больших резервуаров (не менее 100 галлонов), но они полезны, если нет близкого электрического подключения.
Электрические варианты варьируются от погружных до плавающих, от бака до сливной пробки, в зависимости от того, что вы ищете, и обычно стоят менее 150 долларов.
Поддерживать текучесть воды в холодную погоду непросто, но зимой это необходимая работа на ферме. Если вы попробуете какой-либо из неэлектрических вариантов, проверяйте воду хотя бы раз в день, чтобы увидеть, как она работает, и всегда будьте осторожны с пропановыми или электрическими нагревательными элементами в коровниках и рядом с животными.
Предстоящие мероприятия
Зарегистрируйтесь прямо сейчас для повторной сертификации пестицидов и удобрений, если срок действия вашей лицензии истекает в 2022 году.Кредиты будут предлагаться на выставке Ag Pro Expo 27 января в Центре мероприятий Harvest Ridge, а дополнительные возможности будут предлагаться в округе Уэйн 1, 8, 22, 24 и 29 марта. Пожалуйста, позвоните, чтобы узнать время и место проведения.
Хейли Зинда является преподавателем дополнительного образования OSU по сельскому хозяйству и природным ресурсам, с ней можно связаться по телефону 330-264-8722.
Понижение температуры замерзания – это снижение равновесной температуры замерзания.
или температура плавления растворенных веществ в жидкой фазе.Растворенные вещества в
жидкая фаза также повышает равновесную температуру кипения. Давление также
влияет на температуру замерзания (немного) и температуру кипения (сильно).
На этой странице дается простое, не математическое объяснение всех этих
последствия. Хотя явления более общие, вода дается как
знакомый пример, из-за вопросов типа:
- Что происходит с кипячением и замораживанием при добавлении растворенных веществ (например, сахара
или соль) к воде? - Почему дороги посыпают солью, когда идет снег?
- Как работает антифриз?
- Как живые ткани могут выдерживать отрицательные температуры?
- Можно ли заварить хороший чай на вершине горы?
- Работают ли коньки, снижая температуру таяния льда?
(Для тех, кто ищет формальное лечение, эти эффекты
анализируются в стандартных курсах физики второго года обучения под рубриками
фазовых равновесий и уравнения Клаузиуса-Клапейрона, которые мы здесь цитируем
без вывода.)
Почему вещества плавятся и кипятят?
Если немного упростить,
температура является мерой того, сколько энергии содержится в молекулярном движении.
Чтобы начать с явного примера, давайте рассмотрим воду. Когда вода
молекулы достаточно холодные, у них не так много тепловой энергии, поэтому они не
толкаться вокруг слишком много. Следовательно, они могут собираться вместе в очень
организованная структура, называемая льдом. При достаточно высоких температурах они имеют так
много энергии, что они могут избежать притяжения своих соседей.Так
они образуют пар, в котором молекулы разлетаются во все стороны в очень
беспорядочный путь. При средних температурах это означает, что молекулы
иметь умеренное количество энергии (и если давление высокое
достаточно*) они образуют жидкую воду. Здесь у молекул достаточно энергии
передвигаться, но недостаточно, чтобы полностью сбежать от соседей.
Молекулы в жидкой воде более упорядочены, чем в паре, но менее упорядочены.
чем лед.(На примере порядка в жидкости можно заметить, что
центр каждой молекулы находится на расстоянии примерно одного молекулярного диаметра от центра
его ближайших соседей.)
Почему перемена такая внезапная? При атмосферном давлении вода плавится при
0°С и кипит при 100°С. От чего зависит температура плавления и кипения
точка?
Ответ — компромисс между молекулярной энергией (которую мы замечаем
как температура) и молекулярный порядок: разница между высоко
организованная структура во льду, достаточно плотная упаковка в жидкой воде и
почти полная дезорганизация в паре.При 0°С и 100°С порядок
эффект и энергетический эффект точно сбалансированы, поэтому лед и вода
сосуществуют при 0°C, вода и пар сосуществуют при 100°C (при атмосферном
давление).
- Кристаллическую структуру льда довольно трудно показать в двух плоскостях.
размеры, поэтому на рисунках ниже схематично показан более простой
кристаллическая, жидкая и паровая фазы. Узорчатые круги представляют
упрощенно то вещество, при плавлении и испарении которого мы
интересно.Цветные круги представляют собой молекулы воздуха, которые
в основном азот. Черные кружки (следующее изображение) обозначают растворенные вещества.
Эскизы не в масштабе.
Воздействие растворенных веществ
Что произойдет, если вместо чистого
жидкая вода, мы кладем немного соли или сахара в воду? Другими словами, что
если наша жидкая фаза является раствором? Это делает жидкое состояние менее
организованы, потому что молекулы сахара или ионы соли могут свободно перемещаться
почти случайно.Таким образом, молекулы жидкой воды более разупорядочены (менее
регламентировано) в растворе. Лед и пар остаются нетронутыми,
однако: сахар и соль почти не растворяются во льду и не
испаряться около 100°C.
Как это влияет на компромисс между молекулярной энергией и
молекулярный порядок? Прирост беспорядка при испарении теперь меньше, т.к.
жидкая вода в растворе более неупорядочена. Энергетический эффект – это
почти не изменились, поэтому энергетический эффект теперь преобладает над чуть большей
диапазон: молекулы воды в растворе должны иметь несколько больше
энергия (немного более высокая температура), чтобы два эффекта были
в балансе.Поэтому температура кипения раствора выше.
И наоборот, когда мы смотрим на плавление, эффект беспорядка больше для
раствор: при плавлении в раствор молекулы воды переходят из верхней
порядок кристаллического льда в еще более неупорядоченное состояние, чем чистый
жидкость. Поэтому эффект беспорядка может доминировать даже при более низких температурах. Так
температура замерзания ниже для раствора.
Выше я упомянул равновесные температуры замерзания и кипения.Время объяснить. Представьте себе лед, плавающий в чистой воде при температуре 0°С. Если мы добавим немного тепла, часть льда растает. Уберите немного тепла, и часть воды замерзнет. Мы называем это равновесной температурой замерзания: 0°С для воды. Однако, когда кто-то охлаждает достаточно чистую воду, она обычно охлаждается на несколько градусов ниже 0°С, мы говорим, что она переохлаждается на несколько градусов, прежде чем появится первый кристалл льда. Этот ледяной кристалл затем быстро расширяется, выделяя скрытое тепло, которое снова нагревает близлежащую воду примерно до 0°C. Подробнее о переохлаждении и перегреве ниже.
Водный раствор имеет более высокую температуру кипения и более низкую температуру замерзания
точка, чем чистая вода.
Если раствор не слишком концентрированный,
эти два эффекта примерно не зависят от растворенного
вещество: молекула сахара имеет почти такой же эффект, как ион соли. Так,
при условии, что вы не забываете считать каждый ион отдельно, эффект
концентрации при повышении температуры кипения или понижении температуры замерзания.
почти то же самое для всех малых растворенных веществ в воде.(Макромолекулы, такие как
полимеры ведут себя по-разному, потому что у них много соседних растворителей
молекулы и поэтому влияют на растворитель гораздо больше, чем простые растворенные вещества.)
Антифриз. Итак, можно ожидать, что антифриз в
радиатор не только предотвращает его замерзание, но и помогает предотвратить его закипание.
Однако реальная ситуация сложнее: у антифриза
Недостаток в том, что он не так хорошо переносит тепло, как вода.Этиленгликоль является антифризом. Соль используется для таяния снега и льда на
дорогах в холодных странах, но в радиаторах не используется, т.к.
вызывает коррозию и легко кристаллизуется. Сахар не используется в некоторых
приложений, потому что концентрированные растворы сахара вязкие, и
потому что они поддерживают ошибки. Однако многие организмы используют сахара и другие
небольшие органические молекулы в качестве антифриза. См. криобиологию.
Интересное наблюдение: концентрация растворенных веществ в крови меньше, чем в морской воде, поэтому равновесная температура замерзания крови обычно выше, чем у морской воды.Следовательно, некоторые арктические и антарктические рыбы живут при температурах ниже равновесной температуры замерзания нормальной крови. Биоантифриз в их крови — это белок, который работает иначе, чем антифриз, используемый в автомобильных радиаторах: белок антифриза связывается с замерзающими ядрами и, таким образом, позволяет крови оставаться переохлажденной.
Эффект давления
Обратите внимание, что выше я включил оговорку
«при атмосферном давлении» несколько раз.Причина давления
важно то, что в паровой фазе данное количество вещества
занимает гораздо больший объем, чем в жидком виде. Часть энергии
необходимое для испарения, оно направлено на то, чтобы «вытолкнуть воздух с дороги», чтобы
освободить место для испарившегося количества. (объем выполненной работы равен
произведение давления P на изменение объема ΔV. Технически там
является членом PΔV в скрытой теплоте.) Таким образом, при низком давлении легче
образуют паровую фазу, поэтому температура кипения ниже.Зависимость
температура перехода от давления — эффект Клаузиуса-Клапейрона.
(Опять же, будучи немного техническим, отметим, что этот эффект включает в себя энергию —
работа, совершаемая при вытеснении воздуха, тогда как эффект растворенного вещества включает
энтропия — неупорядоченность жидкой фазы.)
Вода сильно расширяется при кипячении: один килограмм воды равен одному литру
жидкой воды, а превращается примерно в 1700 литров пара при атмосферном
давление.Это означает, что даже незначительное увеличение высоты может заметно
снизить температуру кипения. Некоторые люди жалуются, что это влияет
приготовление и даже вкус чая на высоте.
Верно и то, что давление меняет температуру плавления. Тем не мение,
ведь объем, занимаемый килограммом жидкости, мало чем отличается
от того, что занимает килограмм твердого вещества, этот эффект очень мал
если давление не очень большое.Для большинства веществ замораживание
точка поднимается, хотя и очень незначительно, при увеличении давления.
Вода является одним из очень редких веществ, расширяющихся при замерзании.
(вот почему лед плавает). Следовательно, его температура плавления падает очень незначительно при повышении давления.
- Меня спросили: Понижает ли точка замерзания
давлением объяснить низкое трение под коньком? Я пишу это в Сиднее, так что вы можете правильно догадаться, что я мало что знаю о фигурном катании, но давайте попробуем подвести итоги.Уравнение Клаузиуса-Клапейрона говорит, что
отношение изменения давления к изменению удельного объема к
скрытая теплота фазового перехода равна отношению изменения
температура перехода в (абсолютную) температуру плавления или кипения.
Его часто записывают как dP/dT = L/T*Δv. (Как мы могли бы иметь
угадывается из соображений размерности, т. е. просто пишется уравнение с соответствующими параметрами, чтобы единицы измерения были правильными.)
Вес фигуриста, скажем, 1 кН. Я не фигурист, но давайте начнем с оценки площади контакта конька со льдом, скажем, 100 мм 2 . (Значение зависит от того, насколько далеко конек врезается в лед. Скажем, 200 мм в длину и 0,5 мм в ширину: конькобежцы, это разумно?) Таким образом, с этим значением давление увеличивается на (1 кН)/100 мм 2 = 10 МПа или 100 атмосфер. Килограмм воды (один литр) замерзает, чтобы дать
около 1,1 литра льда, поэтому изменение удельного объема составляет примерно
10 -4 м 3 кг -1 .Скрытая теплота
плавления льда 330 кДж.кг -1 . Таким образом, пропорциональное изменение
по температуре
(10 МПа)(10 -4 м 3 кг -1 )/(330 кДж.кг -1 ),
что составляет 0,3%. Умножьте это на температуру таяния льда (273 К).
и для этой области мы получаем оценку изменения температуры около 1 K = 1 °C. Итак, с
этих значений расчет предполагает, что давление конька
понизит температуру таяния льда примерно на
1 °С.Итак, при такой оценке площади и если бы это было причиной скользкости, льда
катание на коньках было бы возможно только при температуре всего один или несколько градусов
ниже точки замерзания. Судя по наблюдению, можно кататься на коньках по льду на
гораздо более низкие температуры, чем это. Чтобы утверждать, что понижение точки замерзания работает при температуре, скажем, 10°C, нам понадобится площадь
контакта конька около 10 мм 2 или менее. Если бы только острые кромки соприкасались со льдом, это могло бы быть возможно, но мне кажется, что это очень мало, потому что давление на лед было бы 100 МПа или 1000 атмосфер, и при таком напряжении я бы ожидал, что кромки врезаться в лед и увеличивать площадь контакта.(Опять же прошу совета по этому поводу у скейтеров, а лучше у физиков, которые тоже скейтеры.)
Если оставить в стороне эффект Клаузиуса-Клапейрона и в условиях лишь небольшого приложенного давления, можно ожидать, что поверхность льда уже несколько
скользко. На поверхности льда у молекул воды есть только возможности для водорода
связи со своими соседями «с одной стороны», так сказать. Следовательно, их энергия
не так низко, как в насыпном льду.Значит, в равновесии они должны иметь более высокое
энтропия. Так, даже при отрицательных температурах лед должен иметь на поверхности тонкий водообразный слой,
толщина, как ожидается, будет увеличиваться при температурах, близких к температуре плавления. [ пс. Спустя несколько лет после написания этой статьи я рад сообщить, что недавнее научное исследование подтверждает идею о том, что поверхностный слой льда делает его скользким, а не понижение точки замерзания. ]
Сопоставимый расчет изменения точки кипения немного больше.
сложный.Скрытая теплота в этом случае больше
(2,3 МДж -1 ), но изменение удельного объема значительно
больше (обычно в несколько раз
10 -2 м 3 кг -1 ). Итак, изменения в
высота может изменить температуру кипения, а подъем в гору может
уменьшить его на несколько градусов.
Когда температура кипения и температура замерзания
равный? Что происходит тогда?
Для всех веществ при понижении давления кипение
температура падает гораздо быстрее, чем температура замерзания.(Для воды температура замерзания немного повышается при низком давлении.)
Отсюда очевидный вопрос: являются ли температура кипения и замерзания
температура всегда одинаковая?
Да. При низком давлении 611 Па (всего 0,006 раз
атмосферное давление), чистая вода кипит при 0,01 °C, а также
замерзает при 0,01 °C. Комбинация условий (P, T) =
(611 Па, 0,01 °C) называется тройной точкой 90 233
вода , потому что при этом давлении и температуре лед, жидкая вода и
пар может сосуществовать в равновесии.Эта точка используется для определения нашей шкалы
температуры: по определению, тройная точка воды находится при
273,16 К, где К – кельвин. 273,16 К = 0,01 °С
* Это объясняет, почему выше я писал, что жидкая вода существует только в том случае, если
давление достаточно высокое. При давлении ниже 611 Па
только две фазы, а лед возгоняется с образованием пара напрямую, минуя
через жидкую фазу. (В этом контексте обратным словом «возвышать» является
а не, как можно было бы надеяться, «высмеивать».При низком давлении пар
конденсируется, образуя лед.

