Сколько соли добавить в раствор при минусовой температуре: Сколько можно сыпать соли в раствор для кладки кирпича? — Стройка и ремонт
- Поваренная соль, раствор, температура замерзания
- Почему лед тает под солью, несмотря на минусовую температуру зимой | Lifestyle
- Противоморозная добавка PolyFrost -15
- Бетонирование с помощью добавок Master Builders Solutions зимой
- При какой температуре замерзает вода – самая полная информация!
- основные способы и инструкции по приготовлению растворов с добавками
- Что представляет собой противоморозная добавка в раствор?
- Антиморозные добавки своими руками
- Проблема организации кирпичной кладки в морозы
- Если бетон замерз, не успев набрать необходимую прочность
- Особенности подготовки раствора
- Как рассчитать дозировку?
- Виды противоморозных добавок
- Мифы, связанные с добавками
- Противоморозная добавка: расход
- Пластификаторы
- Бетонирование при низких температурах
- Что нужно знать о выполнении кладочных работ в зимнее время?
- Принцип действия и виды морозостойких составов
- В итоге
- Бетонирование зимой
- Зачем мы зимой посыпаем солью обледеневшие тротуары?
- Мы все кричим о мороженом
- Почему мы зимой посыпаем дороги солью?
- Может ли вода оставаться жидкой при температуре ниже нуля градусов Цельсия?
- Наука о мороженом — Депрессия точки замерзания
- Уход за лошадью зимой
- Почему морская вода не замерзает при нуле градусов?
Поваренная соль, раствор, температура замерзания
В табл. 11 приведены температуры замерзания (начала кристаллизации) растворов поваренной соли. [c.48]
Растворив в 100 л воды 30,1 кг поваренной соли, мы можем довести температуру замерзания рассола до —21,2°С. Однако дальнейшее повышение концентрации рассола вызывает уже не снижение, а повышение температуры замерзания. Раствор, имеющий наинизшую температуру замерзания, называется эвтектическим (рис. 14). [c.42]
В качестве холодильных рассолов используют водные растворы поваренной соли, хлористого магния и хлористого кальция. Кривые температур замерзания этих растворов показаны на рис. 9.14. По этим кривым выбирают растворы и их концентрации. Например, соответственно приведенным данным раствор хлористого натрия можно рекомендовать для температур не ниже —15°С. Рабочую концентрацию растворов надо выбирать по левой ветви кривой замерзания. Она должна быть на несколько процентов меньше концентрации, соответствующей криогидратной точке. [c.199]
Она должна быть на несколько процентов меньше концентрации, соответствующей криогидратной точке. [c.199]
Наиболее низкую температуру замерзания —21,2° С имеет раствор поваренной соли, содержащий 22,4% Na l. При этой температуре раствор указанного состава полностью замерзает. Из растворов более высокой концентрации при охлаждении сначала кристаллизуется поваренная соль, а из более разбавленных растворов сначала вымерзает вода и, когда концентрация достигает 22,4%) Na l, раствор полностью замерзает. Температуры начала кристаллизации растворов поваренной соли даны в приложении 5. [c.34]
Определение температуры замерзания растворов поваренной соли [c.166]
Коллигативные свойства можно использовать для определения молекулярной массы вещества. Например, если, зная массу т растворенного вещества, определить температуру замерзания (кипения) раствора, то. найдя понижение, повышение) температуры замерзания (кипения) раствора, можно вычислить число молей п раств оренного вещества, а затем и саму молекулярную массу вещества М = т1п. Таким образом можно определить степень диссоциации или ассоциации вещества в растворе. В этом случае следует умножить правую часть уравнений (355) и (356) на введенный Вант-Гоффом в соответствии с уравнением (322) коэффициент . Понижение температуры замерзания раствора повареной соли примерно в два раза больше, чем для раствора сахарозы той же моляльной концентрации. На практике чаще используют криоскопический метод, так как он более прост в экспериментальном исполнении, а кроме того, как правило, криоскопическая константа для одного и того же растворителя больше, чем эбулиоскопическая. Для растворителя камфары, например, =40 К-кг/моль. [c.281]
Таким образом можно определить степень диссоциации или ассоциации вещества в растворе. В этом случае следует умножить правую часть уравнений (355) и (356) на введенный Вант-Гоффом в соответствии с уравнением (322) коэффициент . Понижение температуры замерзания раствора повареной соли примерно в два раза больше, чем для раствора сахарозы той же моляльной концентрации. На практике чаще используют криоскопический метод, так как он более прост в экспериментальном исполнении, а кроме того, как правило, криоскопическая константа для одного и того же растворителя больше, чем эбулиоскопическая. Для растворителя камфары, например, =40 К-кг/моль. [c.281]
Однако на этом этапе ситуация усложнилась. Логично было предположить, что при растворении, например в воде, вещество распадается на отдельные молекулы. Однако наблюдаемое понижение температуры замерзания соответствовало предполагаемому только в тех случаях, когда растворялся неэлектролит, например сахар. При растворении электролита типа поваренной соли ЫаС1 понижение температуры замерзания вдвое превышало ожидаемое, т. е. число частиц, содержащихся в растворе, должно было быть в два раза больше числа молекул соли. А при растворении хлорида бария ВаСи число частиц, находящихся в растворе, должно было превышать число молекул втрое. [c.119]
е. число частиц, содержащихся в растворе, должно было быть в два раза больше числа молекул соли. А при растворении хлорида бария ВаСи число частиц, находящихся в растворе, должно было превышать число молекул втрое. [c.119]
Во избежание просаливания рыбы при замораживании применяют раствор поваренной соли с температурой, близкой к точке его замерзания, т. е. осмотически пассивный и почти исключающий возможность проникновения соли в ткани рыбы. Криогидратная температура раствора поваренной соли равна —21,2°, а следовательно, практически рассол может быть охлажден только до температуры —18°, при которой рыба обычно замораживается до [c.121]
Водные растворы солей. Классическим примером бинарной смеси с одним компонентом в одной из фаз может служить водный раствор поваренной соли (рис. 13,г). В состоянии А раствор концентрации = 1а при температуре tл является жидким. При / = 0° С и р = 1 атм он еще не замерзает, и только при более низкой температуре в точке Я образуются первые кристаллы льда, часть воды, вымерзая, переходит в твердую фазу, концентрация остаточного раствора постепенно увеличивается, и точка замерзания понижается. В точке Я устанавливается равновесие между жидким раствором концентрации и первыми кристаллами чистого льда ( = 0), причем обе фазы имеют одинаковые температуру и давление. Состояние смеси при дальнейшем охлаждении постепенно изменяется (от точки Я до Р) и тогда выпадает новая порция льда, а жидкая часть становится более концентрированной и достигает точки О, где раствор снова находится в равновесии, но уже при более низкой температуре. Кривая равновесия ВНОЕ — является кривой льда (40]. [c.37]
В точке Я устанавливается равновесие между жидким раствором концентрации и первыми кристаллами чистого льда ( = 0), причем обе фазы имеют одинаковые температуру и давление. Состояние смеси при дальнейшем охлаждении постепенно изменяется (от точки Я до Р) и тогда выпадает новая порция льда, а жидкая часть становится более концентрированной и достигает точки О, где раствор снова находится в равновесии, но уже при более низкой температуре. Кривая равновесия ВНОЕ — является кривой льда (40]. [c.37]
Все химически чистые вещества имеют определенные температуры (точки) замерзания и кипения вода замерзает при 0° и кипит ири 100 С (имеется в виду нормальное давление). У растворов этого пе наблюдается, они отличаются от чистых растворителей по свойствам. Присутствие растворенного вещества понижает температуру замерзания и повышает температуру кппенпя раствора. Поэтому водные растворы замерзают прп более низкой температуре, чем чистая вода. Чем копцентрированнее раствор, тем ниже точка его замерзания.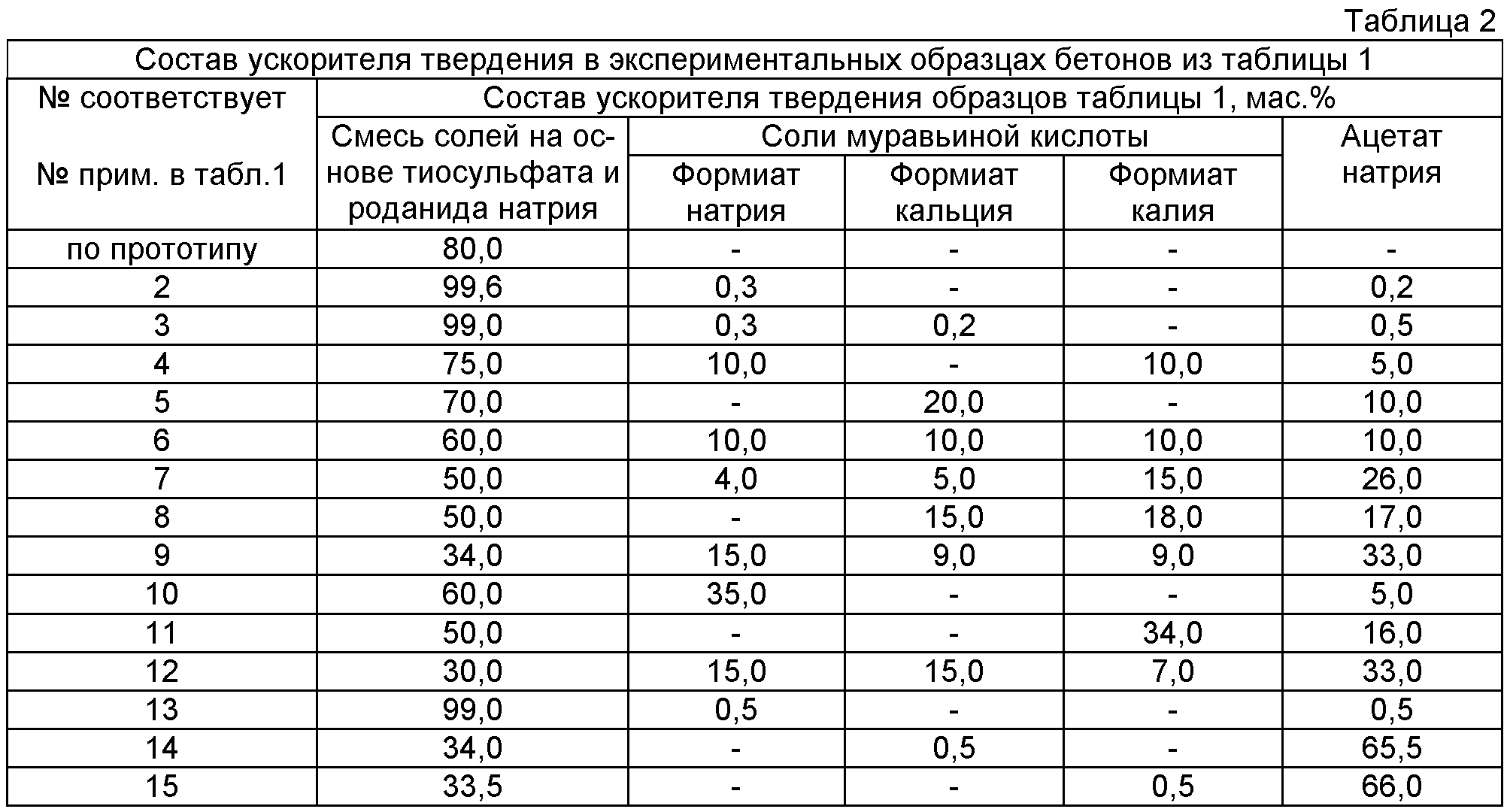 Например, если в 100 г воды растворено 10 г поваренной соли, то раствор замерзает при —13,6 , а если растворить 30 г Na l, то он будет замерзать при —21,2 °С. Подобно этому, температура кипения водных растворов лежит выше 100 °С и зависит от копцептрацпи. Так, если в 100 г воды растворить 21 г хлористого кальция, то раствор закипит при 104 , а если растворить 69 г a L, — то при 120 °С. [c.113]
Например, если в 100 г воды растворено 10 г поваренной соли, то раствор замерзает при —13,6 , а если растворить 30 г Na l, то он будет замерзать при —21,2 °С. Подобно этому, температура кипения водных растворов лежит выше 100 °С и зависит от копцептрацпи. Так, если в 100 г воды растворить 21 г хлористого кальция, то раствор закипит при 104 , а если растворить 69 г a L, — то при 120 °С. [c.113]
Для этой цели пользуются в качестве охлаждающей жидкости водными растворами солей, чаще всего поваренной соли. Такие растворы замерзают при температурах ниже 0°. Чем больше концентрация раствора соли, тем ниже (до известного предела) температура его замерзания. Обычно пользуются рассолом, содержащим около 20% соли и замерзающим при температуре —18°. Рассол предварительно охлаждают в специальной холодильной установке до температуры от —12° до —15° и затем подают в рубашки или змеевики охлаждаемых аппаратов. Воду и рассол вводят в рубашку или змеевик снизу, а отводят сверху. [c.97]
[c.97]
В погружных испарителях в качестве вторичного теплоносителя применяют водный раствор поваренной соли с удельным весом 1,16 и температурой замерзания —18,2°. При закрытых испарителях используют водный раствор хлористого кальция с удельным весом 1,22 и температурой замерзания —25,7°. [c.375]
В 1753—1756 гг. М. В. Ломоносов провел экспериментальные исследования водных растворов. Он был одним из первых ученых, поставивших себе целью изучить растворимость солей в воде при различных температурах. Им была изучена растворимость многих солей при различных температурах. М. В. Ломоносов наблюдал зависимость температуры замерзания растворов от количества растворенной соли. Он опытным путем установил, например, что растворы поваренной соли (а также морская вода) замерзают тем ниже, чем концентрированнее раствор. [c.17]
Хлорид натрия Na l (поваренная соль, галит, каменная соль) — белые кристаллы. Получается путем выпаривания рассолов и добычи в твердом состоянии. Используется без всякой обработки или в виде приготовленного солевого раствора при заканчивании и капитальном ремонте скважин (см. главу 10) для приготовления насыщенного водного раствора для разбуривания каменной соли для снижения температуры замерзания бурового раствора для повышения плотности (в виде взвешенной твердой фазы) в качестве закупоривающего материала в насыщенных растворах, а также в повышающих устойчивость ствола буровых растворах на углеводородной основе (см. главы 8 и 9). Концентрации от 30 до 360 кг/м . Потребление в 1978 г. 60 тыс. т. [c.496]
Используется без всякой обработки или в виде приготовленного солевого раствора при заканчивании и капитальном ремонте скважин (см. главу 10) для приготовления насыщенного водного раствора для разбуривания каменной соли для снижения температуры замерзания бурового раствора для повышения плотности (в виде взвешенной твердой фазы) в качестве закупоривающего материала в насыщенных растворах, а также в повышающих устойчивость ствола буровых растворах на углеводородной основе (см. главы 8 и 9). Концентрации от 30 до 360 кг/м . Потребление в 1978 г. 60 тыс. т. [c.496]
Температура кипения и з аме р з а н и я растворов. Растворы твердых веществ закипают при более высокой температуре и замерзают при более низкой температуре, чем чистые растворители. Морская вода, воды соленых озер замерзают несколько ниже 0°, а кипят несколько выше 100°. Лед может существовать при 0°, но известно, что если лед посыпать поваренной солью, то он начнет таять. Температура замерзания раствора поваренной соли лежит ниже той температуры, при которой находится лед, поэтому он ве может оставаться в твердом состоянии вместе с поваренной солью и тает. При таянии льда происходит большое поглощение теплоты, вызывающее сильное охлаждение. Это обстоятельство часто используется в химических и других работах для искусственного получения низких температур. С этой целью готовят специальные охлаждающие смеси . Смесью 3 весовых частей снега или толченого льда с одной весовой частью поваренной соли Na l достигается снижение температуры до—22°. Смесью одной части снега с 1,4 части хлорида кальция a lj eHjO достигается снижение температуры до —55°. [c.64]
При таянии льда происходит большое поглощение теплоты, вызывающее сильное охлаждение. Это обстоятельство часто используется в химических и других работах для искусственного получения низких температур. С этой целью готовят специальные охлаждающие смеси . Смесью 3 весовых частей снега или толченого льда с одной весовой частью поваренной соли Na l достигается снижение температуры до—22°. Смесью одной части снега с 1,4 части хлорида кальция a lj eHjO достигается снижение температуры до —55°. [c.64]
При отрицательной температуре воздуха гидравлические испытания аппаратов производят с помощью подогретой паром воды или специальных водных растворов, имеющих низкую температуру замерзания. Обычно для этих целей используют растворы хлористого кальция или хлористого натрия (поваренную соль) [c.42]
Температура таяния льдосоляной смеси и ее охлаждающий эффект, т. е. холодопронзводительность, зависят от количества и сорта соли, находящейся в смеси. При использовании технической поваренной соли (ЫаС1) температура охлаждения может достигнуть — 16-г—18 С, при использовании хлористого кальция (СаС12) — более низких температур (—46- —48° С). С повышением содержания соли в льдосоляной смеси температура ее плавления и равная ей температура замерзания раствора соответствующей концентрации понижается. Раствор соли с наи-низшей температурой замерзания называется эвтектическим, а температура замерзания эвтектического раствора, называется криогидратной температурой или криогидратной точкой. [c.28]
При использовании технической поваренной соли (ЫаС1) температура охлаждения может достигнуть — 16-г—18 С, при использовании хлористого кальция (СаС12) — более низких температур (—46- —48° С). С повышением содержания соли в льдосоляной смеси температура ее плавления и равная ей температура замерзания раствора соответствующей концентрации понижается. Раствор соли с наи-низшей температурой замерзания называется эвтектическим, а температура замерзания эвтектического раствора, называется криогидратной температурой или криогидратной точкой. [c.28]
Известно, что растворенные в воде вещества, в том числе поваренная соль и сахар (сахароза), понижают температуру замерзания растворов. Поэтому можно не бояться охлаждения банок с вареньем или солеными огурцами на 1—2 градуса ниже нуля, это не принесет вреда. Но при сильном морозе консервы могут замерзнуть, и хотя пищевая ценность при этом не изменится, внешний вид и вкус продукта пострадают непоправимо кристаллы льда повредят оболочки растительных клеток, сок вытечет, фрукты и овощи станут мягкими и дряблыми. Перемороженные огурцы годятся разве что на рассольник. [c.68]
Перемороженные огурцы годятся разве что на рассольник. [c.68]
Экспериментально измеренное осмотическое давление растворов солей, кислот и оснований оказывается всегда больше теоретически рассчитанного. Наоборот, молекулярный вес этих веществ, рассчитанный по повышению температуры кипения или по понижению температуры замерзания растворов, меньше теоретического. Так, теоретический молекулярный вес (масса) поваренной соли 58,5, а измеренный криоскопическим методом — 30,1. Молекулярный вес хлористого калия, вычисленный по повышению температуры кипения раствора, равен 38,7, а теоретический — 74,5. [c.172]
Свойство поваренной соли понижать в растворе температуру замерзания воды с древних времен используется для борьбы с гололедом на дорогах. Предприятия коммунального и дорожного хозяйства в зимнее время года давно применяют поваренную соль для посыпки дорог, для предупреждения аварий и травматизма. На посыпку дорог используется в основном попутная соль калийных производств. По данным ГИПРОДОРНИИ, потребность в поваренной соли только для автодорожных предприятий РСФСР к 1990 г. составит 1,8 млн. т/год. [c.16]
По данным ГИПРОДОРНИИ, потребность в поваренной соли только для автодорожных предприятий РСФСР к 1990 г. составит 1,8 млн. т/год. [c.16]
Температура охлаждающей воды, текущей по змеевикам и другим охлаждающим элементам, не может быть ниже 0°, так как при олее низкой температуре она замерзает. При необходимости иметь более низкие температуры пользуются в качестве охлаждающей жидкости не чистой водой, а водными растворами солей, чаще всего поваренной соли. Такие растворы замерзают при температурах ниже 0°, причем чем крепче раствор, тем ниже (До извест ного предела) его температура замерзания. На практике обычно пользуются рассолами крепостью приблизительно 20%, замерзающими при температуре около —18°. Охлаждение таких рассолов производится на специальных холодильных установках, откуда рассол с температурой обыч.чо от —12° до —15° подается центробежными насосами в охлаждающие элементы аппаратов — змеевики, рубашки, 228 [c.228]
Известно, что температура замерзания растворителя понижается при растворении в нем нелетучего вещества. Например, вода, замерзающая при О °С, не замерзает при той же температуре в том случае, когда в нее добавлена поваренная соль или хлористый кальций, температура замерзания понижается. Вообще, растворы замерзают при более низких температурах, чем чистые растворители. Эффект понижения температуры замерзания жидкости при растворении в ней твердого вещества используется в методе криоскопии. Заметим, что величина, на которую понижается температура замерзания, зависит от числа молекул растворенного вещества в единице объема раствора и не зависит от их размеров (массы) и химической природы. Это означает, что если метод криоскохши применяют для определения молекулярной массы полимера, то получается среднечисловая молекулярная масса М . Если обозначить снижение температуры замерзания как ДГотв> то его связь с М и концентрацией определяется следующим уравнением [c.304]
Например, вода, замерзающая при О °С, не замерзает при той же температуре в том случае, когда в нее добавлена поваренная соль или хлористый кальций, температура замерзания понижается. Вообще, растворы замерзают при более низких температурах, чем чистые растворители. Эффект понижения температуры замерзания жидкости при растворении в ней твердого вещества используется в методе криоскопии. Заметим, что величина, на которую понижается температура замерзания, зависит от числа молекул растворенного вещества в единице объема раствора и не зависит от их размеров (массы) и химической природы. Это означает, что если метод криоскохши применяют для определения молекулярной массы полимера, то получается среднечисловая молекулярная масса М . Если обозначить снижение температуры замерзания как ДГотв> то его связь с М и концентрацией определяется следующим уравнением [c.304]
Для выполнения эксперимента необходимы следующее оборудование и реактивы прибор для определения понижения температуры замерзания водных растворов бюретка для титрования — 2 шт. пипетка на 15 мл пипетка на 10 мл колба для титрования на 100 мл снег или лед поваренная соль раствор 0,6 М USO4 в 5 М растворе аммиака раствор HG1 0,1 М раствор NaOH 0,1 М раствор метилоранжа 20%-ный раствор KI раствор ЫагЗгОз 0,1 М раствор крахмала. [c.353]
пипетка на 15 мл пипетка на 10 мл колба для титрования на 100 мл снег или лед поваренная соль раствор 0,6 М USO4 в 5 М растворе аммиака раствор HG1 0,1 М раствор NaOH 0,1 М раствор метилоранжа 20%-ный раствор KI раствор ЫагЗгОз 0,1 М раствор крахмала. [c.353]
При замерзании рассола с концентрацией ниже криогидратной точки сна-члт выделяется лед, поэтому левую ветвь можно назвать кривой выделения льда. Например, если охлаждать раствор поваренной соли, имеюпщй концентрацию 15%, то до температуры —11°С (точка а) концентрация его будет постоянной, а при дальнейшем охлажде- W 20 30 40 НИИ начнется выделение льда. Концентрация оставшегося жидкого раствора р с. и. Диаграмма темпера-будет увеличиваться по левой ветви кри- тур затвердевания рассолов, вых, а температура затвердевания будет [c.35]
В качестве рассолов применяют водные растворы хлористого натрия N801 (поваренной соли) и хлористого кальция СаСЬ, которые имеют достаточно низкие температуры замерзания и дешевы. Растворы пригодны для использования лишь при температурах, превышающих те, при которых они замерзают как однородная смесь, образуя соленый лед (криогидратная точка). Криоги-дратной точке для раствора ЫаС1 с концентрацией 22,4% (по весу раствора) соответствует температура минус 21,2° С, а для раствора СаСЬ с концентрацией 29,9%—температура минус 55° С. Поэтому для получения низких температур применяется СаСЬ. [c.245]
Растворы пригодны для использования лишь при температурах, превышающих те, при которых они замерзают как однородная смесь, образуя соленый лед (криогидратная точка). Криоги-дратной точке для раствора ЫаС1 с концентрацией 22,4% (по весу раствора) соответствует температура минус 21,2° С, а для раствора СаСЬ с концентрацией 29,9%—температура минус 55° С. Поэтому для получения низких температур применяется СаСЬ. [c.245]
Характерным для рассолов, как это показано на рис. 7.1, является следующее. При температуре замерзания из рассолов, концентрация которых менее 22,4% Na I, выпадают кристаллы льда, не содержащие поваренной Обсоли. Поэтому по мере охлаждения gg таких рассолов концентрация Na l в растворе возрастает, при ми-нус 21,2 °С содержание поварен-ной соли в растворе достигает [c.227]
При колонковом буренпп скважин в устойчивых породах может быть применена промывка водой. При бурении скважин в породах малоустойчивых (пористых и сыпучих) промывка осуществляется глинистым раствором. При бурении в вечной мерзлоте приходится пршменять сильно охлажденные растворы поваренной соли в глинистом растворе с температурой замерзания более низкой, чем температура почвы. [c.8]
При бурении в вечной мерзлоте приходится пршменять сильно охлажденные растворы поваренной соли в глинистом растворе с температурой замерзания более низкой, чем температура почвы. [c.8]
Таким образом, замерзание растворов солей, а следовательно, и плавление льдосоляных смесей, происходит при переменной температуре, величина которой связана с концентрацией соли в жидкой фазе. Только раствор состояния 3, имеющий эвтектическую концентрацию д, при достаточном охлаждении замерзает при постоянной температуре 4, а замороженный раствор эвтектической концентрации, называемый эвтектическим льдом или звтек-тиком, плавится при этой же постоянной и наинизшей температуре для смесей льда и данной соли. Так, смесь льда и хлорида калия, содержащая 19,3% по массе соли, представляет собой эвтектическую смесь, плавящуюся при температуре —11,Г С эвтектическая смесь льда и поваренной соли содержит 23,1% соли и плавится при температуре —21,2° С эвтектическая смесь льда и хлорида кальция, в составе которой 29,9% соли, плавится при —55° С.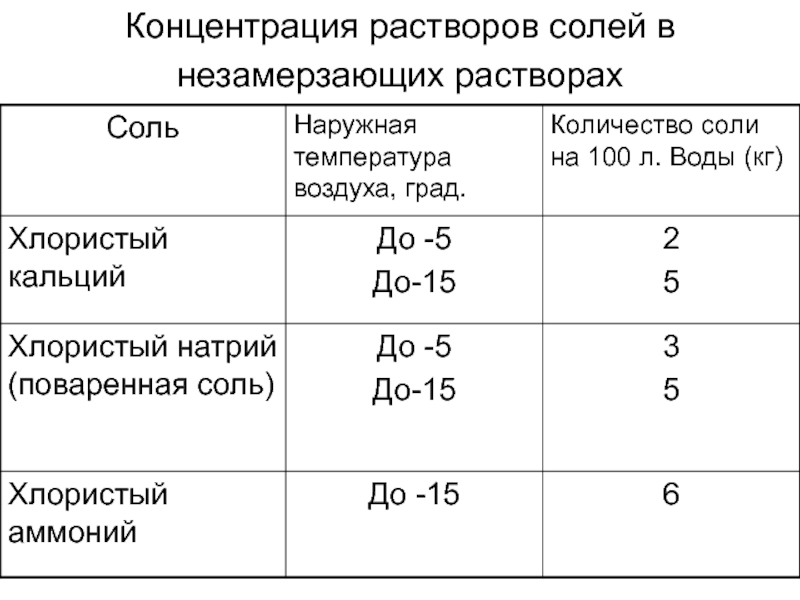 На рис. 10.6 область Л Р между линией А и изотермой эвтектической температуры t , отвечает сосуществованию двух фаз льда и раствора. Соотношение между массами отдельных фаз определяется, как в любых двухфазных системах, по правилу рычага. В свою очередь, область С + Р соответствует двухфазному состоянию смеси соли и раствора. При температурах ниже эвтектической смеси льда и соли могут существовать только в твердом состоянии. Область Л + Э является зоной существования смеси льда и эвтектика, а область С + Э — смеси соли и эвтектика. [c.322]
На рис. 10.6 область Л Р между линией А и изотермой эвтектической температуры t , отвечает сосуществованию двух фаз льда и раствора. Соотношение между массами отдельных фаз определяется, как в любых двухфазных системах, по правилу рычага. В свою очередь, область С + Р соответствует двухфазному состоянию смеси соли и раствора. При температурах ниже эвтектической смеси льда и соли могут существовать только в твердом состоянии. Область Л + Э является зоной существования смеси льда и эвтектика, а область С + Э — смеси соли и эвтектика. [c.322]
Почему лед тает под солью, несмотря на минусовую температуру зимой | Lifestyle
Вы знаете, что можно посыпать солью обледеневшую дорогу или тротуар, чтобы в дальнейшем на них никто не поскользнулся? Но известно ли вам, как соль плавит лед? Что такое депрессия точки замерзания и как она работает, выясним в статье.
Почему лед тает под солью
Замерзшая вода тает под солью ввиду таких причин:
- Соль помогает предотвратить повторное превращение воды в лед путем понижения температуры ее трансформации.
 Это явление называют депрессией точки замерзания.
Это явление называют депрессией точки замерзания. - Диапазон рабочих температур не одинаков для всех видов соли. Например, хлорид кальция понижает температуру застывания больше, чем хлорид натрия.
- В дополнение к таянию льда депрессия точки замерзания может использоваться, чтобы изготовить мороженое без морозильника.
Депрессия точки замерзания
Соль растворяет лед ввиду того, что она понижает точку замерзания воды. Так каков этот процесс? Лед начнет таять лишь в том случае, если на его поверхности есть немного жидкости. Хорошей новостью является то, что вам не нужна большая лужа для достижения результата. Лед обычно покрыт тонкой водяной пленкой, и это все, что требуется.
Чистая вода застывает при 0°C. Вода с солью (или любой иной субстанцией) заледенеет, когда температура будет более низкой. Насколько должно быть холодно, зависит от агента, ликвидирующего гололед. Если вы бросите соль на лед тогда, когда температура не собирается подниматься до новой точки застывания соленого раствора, вы не получите выгоды.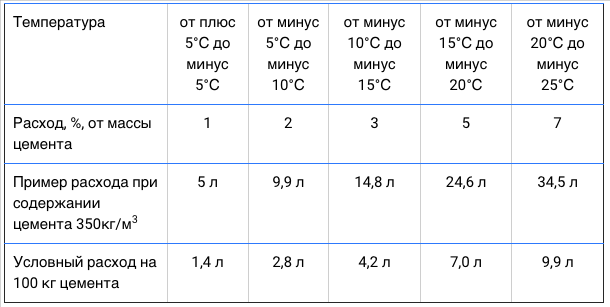 Например, если вы бросите столовую соль (натрия хлорид) на лед, когда на улице -17°С, то вы просто покроете лед слоем соли. Но если вы ту же соль положите на лед при температуре -9,5°С, вы сможете предотвратить вторичное застывание тающего льда. Магния хлорид работает до -15°С, а хлорид кальция – до -28,8°С.
Например, если вы бросите столовую соль (натрия хлорид) на лед, когда на улице -17°С, то вы просто покроете лед слоем соли. Но если вы ту же соль положите на лед при температуре -9,5°С, вы сможете предотвратить вторичное застывание тающего льда. Магния хлорид работает до -15°С, а хлорид кальция – до -28,8°С.
Если температура снизится до той отметки, на которой солевой раствор может замерзнуть, энергия будет освобождаться и появятся связи, благодаря которым жидкость заледенеет. Этой энергии хватит, чтобы растопить немного чистого льда и продолжить процесс таяния.
Изготовление мороженого
Вы можете самостоятельно реализовать эффект понижения температуры замерзания, даже если у вас нет рядом заледеневшей дороги. Одним из способов является приготовление собственного мороженого в пакете, где смешивание соли с водой приводит к получению очень холодной смеси. Если вы хотите выяснить, как можно холодный лед получить с помощью соли, смешайте 0,935 кг обычной столовой соли с 2,8 кг колотого льда или снега. Будьте осторожны! Температура смеси опустится до -21°C, что может вызвать обморожение, если вы будете долго держать ее в руках.
Будьте осторожны! Температура смеси опустится до -21°C, что может вызвать обморожение, если вы будете долго держать ее в руках.
Поваренная соль делится в воде на ионы натрия и хлорида. Сахар в воде растворяется, но на ионы не распадается. И все же добавление сахара в воду тоже влияет на температуру замерзания.
Другие субстанции
Реакция соли с водой не единственная, которая вызывает замерзание. Каждый раз, когда вы частицы добавляете в жидкость, температура замерзания снижается, а температура кипения повышается. Еще один отличный пример снижения температуры замерзания — водка. Этот алкогольный напиток содержит и воду, и этанол. В домашней морозилке обычно водка не превращается в лед, так как спирт понижает температуру видоизменения воды.
Противоморозная добавка PolyFrost -15
Твердение бетонов и растворов при пониженной температуре происходит медленно, так как замедляется процесс гидратации цемента. Уже при температуре ― 3…- 6 °С вода в бетоне замерзает, и процессы гидратации вяжущего и твердения бетона практически прекращаются. При оттаивании, при условии сохранения жидкой фазы, эти процессы возобновляются, и бетон продолжает увеличивать свою прочность. Однако для бетона, замороженного в раннем возрасте, после оттаивания и последующей выдержки характерны рыхлая структура, низкая прочность и морозостойкость. Это объясняется тем, что свежеуложенный бетон содержит много воды, которая при замерзании расширяется, разрыхляет цементный камень и нарушает сцепление заполнителя с цементной матрицей.
При оттаивании, при условии сохранения жидкой фазы, эти процессы возобновляются, и бетон продолжает увеличивать свою прочность. Однако для бетона, замороженного в раннем возрасте, после оттаивания и последующей выдержки характерны рыхлая структура, низкая прочность и морозостойкость. Это объясняется тем, что свежеуложенный бетон содержит много воды, которая при замерзании расширяется, разрыхляет цементный камень и нарушает сцепление заполнителя с цементной матрицей.
Поэтому для обеспечения требуемого набора прочности бетона в зимнее время необходимо создавать такие условия, при которых будут активно протекать процессы твердения вяжущего, т. е. необходимо обеспечивать наличие жидкой фазы. Эту задачу можно решить, например, путем выдерживания забетонированной конструкции при положительной температуре. Такое выдерживание можно осуществлять при обогреве бетона в термоактивной опалубке, использованием разогретых смесей с последующим укрытием поверхности конструкции теплоизоляционными материалами и другими способами.
В тех случаях, когда на строительной площадке по техническим или организационным причинам такие способы не могут быть реализованы, целесообразно в бетон вводить противоморозные добавки — вещества, понижающие температуру замерзания воды и способствующие твердению бетона при отрицательных температурах.
Применение бетонов с противоморозными добавками осуществляется при возведении монолитных бетонных и железобетонных сооружений, монолитных частей сборно-монолитных конструкций, замоноличивании стыков сборных конструкций, при изготовлении сборных бетонных и железобетонных изделий и конструкций в условиях полигона при установившейся среднесуточной температуре наружного воздуха и грунта не ниже 5 °С и минимальной суточной температуре ниже 0 °С.
В настоящее время наиболее эффективными и проверенными в производственных условиях противоморозными добавками являются добавки европейских, турецких, российских и белорусских производителей.
Все перечисленные добавки одновременно являются и добавками-ускорителями схватывания и твердения бетонов и растворов, однако их концентрация в «холодных» бетонах значительно (в 2-3 раза) превышает ту, которая необходима для ускорения процессов твердения бетонов при температуре выше 0 °С.
Противоморозные добавки допускаются к применению в тяжелых и легких бетонах. Ориентировочный расход противоморозных добавок в зависимости от расчетной температуры твердения бетона составляет 2-5% для сухого вещества и 4-7% в жидком виде от массы сухого цемента.
Процесс кристаллизации солей происходит с увеличением объёма, поэтому их накопление в отдельных зонах конструкций может привести к дефектам и разрушению этих зон. Опасными в этом отношении являются, добавки, содержащие поташ и нитрат кальция. В следствии активного участия ряда добавок в процессах гидратации цемента, оптимальное их количество для той или иной отрицательной температуры, а также скорость твердения бетона на морозе в значительной мере зависят от минералогического и вещественного состава цемента.
Вид противоморозной добавки выбирается в зависимости от типа и условий эксплуатации конструкций, темпа строительства, метеорологических условий (температуры наружного воздуха и скорости ветра) и технико-экономических показателей.
Количество выбранной противоморозной добавки для получения требуемого снижения температуры замерзания воды устанавливается в зависимости от класса бетона или марки раствора, марки или активности цемента, подвижности бетонной или растворной смеси, предельной крупности и зернового состава заполнителя. При этом, количество добавки, вводимой с целью предотвращения замерзания воды затворения и воды, поглощаемой крупным заполнителем, назначается не от массы цемента, как величины при прочих равных условиях переменной, а от расхода воды затворения бетонной смеси.
Для правильного дозирования и равномерного распределения противоморозные добавки следует вводить в бетонную смесь в виде водного раствора рабочей концентрации, т. е. раствора, которым затворяется смесь без дополнительного введения в неё воды. Требуемая концентрация рабочего раствора устанавливается при подборе состава бетона.
е. раствора, которым затворяется смесь без дополнительного введения в неё воды. Требуемая концентрация рабочего раствора устанавливается при подборе состава бетона.
Расход противоморозной добавки устанавливается по формуле:
Д = В · Дт.п., кг/м3,
где В ― расход воды для затворения бетонной смеси, л/м3;
Дт.п. — содержание сухого вещества (твердого продукта) противоморозной добавки в 1 л водного раствора заданной концентрации в зависимости от требуемой температуры замерзания воды, кг/л.
Расход противоморозной добавки Д, определенный по вышеприведенной формуле, следует проверять и сопоставлять с нормативными допусками её содержания в бетоне (С) в зависимости от расхода цемента:
С = Д · 100/Ц, %,
где Ц ― расход цемента на 1 м3 бетона, кг.
Если установленное количество С превышает предельно допустимое содержание добавки в бетоне, то такую добавку можно применять только с добавлением ингибиторов коррозии стали.
При поставке противоморозной добавки в жидком виде (концентрированный раствор) раствор рабочей концентрации приготовляется смешиванием добавки с водой затворения. Если добавка доставляется в виде твердого продукта или в пастообразном состоянии, то раствор рабочей концентрации может приготовляться путем растворения добавки в заданном количестве воды, либо сначала готовится концентрированный раствор добавки, который затем разбавляется водой.
При приготовлении раствора рабочей концентрации необходимое количество добавки для получения раствора требуемой концентрации определяется по данным Руководства в зависимости от содержания безводного продукта в 1 л раствора определенной плотности.
При выборе дозировок добавок следует учитывать следующие ограничения:
при работе на холодных материалах в бетоны с водоцементным отношением В/Ц < 0,5 необходимо назначать меньшее из указанных пределов количество добавок, а в бетоны с В/Ц > 0,5 — большее;
в бетоны на портландцементах, содержащих С3А более 6 %, при работе на подогретых заполнителях следует вводить меньшее количество добавок, а при содержании в портландцементах С3А меньше 6 % следует вводить меньшее количество.
Назначение оптимального количества противоморозной добавки имеет важное значение, так как при недостаточном ее количестве может произойти преждевременное замерзание бетона, а при избыточном — темп твердения бетона может замедлиться и неоправданно увеличивается стоимость бетона.
Применение бетонов с противоморозными добавками осуществляется при возведении монолитных бетонных и железобетонных сооружений, монолитных частей сборно-монолитных конструкций, замоноличивании стыков сборных конструкций, при изготовлении сборных бетонных и железобетонных изделий и конструкций в условиях полигона при установившейся среднесуточной температуре наружного воздуха и грунта не ниже 5 °С и минимальной суточной температуре ниже 0 °С.
Сущность технологии зимнего бетонирования заключается в том, что растворы солей, введенные в бетонную смесь при ее приготовлении, в процессе выдерживания уложенного в конструкцию бетона, имеющего положительную начальную температуру, значительно продлевают состояние жидкой фазы, обеспечивая тем самым протекание реакции гидратации даже в условиях отрицательных температур. К числу используемых солей относятся нитрит натрия, нитрит кальция, поташ, хлористый натрий и др.
К числу используемых солей относятся нитрит натрия, нитрит кальция, поташ, хлористый натрий и др.
Область применения данной технологии — бетоны в конструкциях, армированных нерасчетной арматурой с защитным слоем бетона не менее 50 мм. Количество противоморозных добавок определяют в процентном отношении к массе цемента. Подбор состава бетона с требуемыми добавками осуществляют с учетом типа и условий эксплуатации монолитной конструкции, температуры наружного воздуха. Количество вносимых добавок увеличивается при возрастании значения отрицательной температуры относительно расчетной.
Применению бетонов с противоморозными добавками должно предшествовать испытание образцов на коррозийное воздействие добавок на бетон, образование высолов на наружной поверхности бетона, скорость твердения бетона и его прочностные характеристики
Температура бетона с противоморозными добавками к началу выдерживания должна оставаться положительной. Ее значение должно превышать температуру наружного воздуха не менее чем на 5°С со знаком «+» (температура воздуха — 13°С, температура укладываемого бетона не менее +18°С). Незаопа-лубленные поверхности монолитных конструкций должны быть теплоизолированы для предотвращения вымораживания влаги с этих участков.
Незаопа-лубленные поверхности монолитных конструкций должны быть теплоизолированы для предотвращения вымораживания влаги с этих участков.
При ведении бетонных работ без искусственного обогрева контролю подвергают:
• условия бетонирования и начальную температуру укладываемой бетонной смеси;
• среднюю температуру бетона в период выдерживания;
• продолжительность остывания бетона до 0°С при методе «термоса» и до расчетной минусовой температуры при использовании противоморозных добавок;
• теплоизолирующее покрытие конструкции, его соответствие требуемому значению теплопередачи;
• максимальную глубину оттаивания основания и отогрева смежного с бетонируемым участка ранее уложенного бетона (ранее имевших температуру наружного воздуха), на которые будет укладываться бетонная смесь;
• резкое изменение температурных условий твердения бетона, требующее принятия дополнительных оперативных мер для обеспечения получения критической прочности бетона до его замерзания. К таким мерам относятся устройство дополнительной теплоизоляции бетона, продление сроков его выдерживания, при необходимости, применение искусственного прогрева конструкции.
К таким мерам относятся устройство дополнительной теплоизоляции бетона, продление сроков его выдерживания, при необходимости, применение искусственного прогрева конструкции.
Безобогревные методы зимнего бетонирования имеют хорошие перспективы для применения. Их прогресс основывается на разработке новых теплоизоляционных материалов, обеспечивающих надежную изоляцию свежеуложенного бетона в конструкцию любой формы, внедрении новых недорогих и эффективных добавок — ускорителей твердения бетона, одновременно являющихся противоморозными, в обеспечении оперативных расчетов и автоматического контроля за условиями выдерживания бетона.
Бетонирование с помощью добавок Master Builders Solutions зимой
Бетонирование при отрицательных температурах
Один из самых главных вопросов зимой: «Зачем нужны противоморозные добавки (ПМД)?»
С понижением температуры ниже +15°С скорость реакции гидратации цемента сильно снижается. При +5°С она измеряется уже не часами, как, например, летом, а сутками, а при 0°С и ниже — останавливается вообще.
В купе с образованием льда при отсутствии прогрева и замораживании структура бетона разрушается, и дальнейший набор прочности может быть очень сильно ограничен.
Многие спрашивают: если применить противоморозные добавки, то бетон можно не греть зимой?
К сожалению, это заблуждение. Уход (прогрев) за свежеуложенным бетоном необходим при пониженных температурах.
Согласно ГОСТ 24211-2008 даже при использовании ПМД для «холодного бетона и раствора» их эффективность может измеряться в пределах 30%-40% от прочности бетона в нормальных условиях в 28 суток. Что это значит – вместо ожидаемых 32 МПа для класса В25 на 28 сутки мы увидим прочность около 11-15 МПа. Дальнейший набор прочности будет очень медленным. Очевидно, что данный вариант подходит только для специальных задач и условий.
Именно поэтому мы рекомендуем рассматривать применение противоморозных добавок в разрезе т.н. «теплого» бетона по ГОСТ 24211-2008. Это бетон или раствор, изготовленный из бетонной или растворной смеси с противоморозной добавкой, обеспечивающей незамерзание смеси при отрицательной температуре на время от ее изготовления до начала обогрева забетонированной конструкции (в течение 4 часов при -18 °С). Тогда на 28 сутки вы гарантированно получите прочность 95% от нормального твердения.
Тогда на 28 сутки вы гарантированно получите прочность 95% от нормального твердения.
Зачем тогда нужны противоморозные добавки?
- Применение противоморозных добавок в виде растворов солей позволяет снизить температуру замерзания воды в капиллярах. Чем меньше размеры пор и капилляров в бетоне, тем ниже в них температура замерзания воды затворения. Даже при небольшой концентрации солей данный механизм позволяет сохранить жидкую фазу в порах бетона даже при низкой отрицательной температуре. Этот механизм позволяет бетону набирать прочность.
Однако, противоморозные добавки не помогут против замерзания смеси! Количество вводимых добавок слишком мало, чтобы снизить точку замерзания всей воды в бетонной смеси. Именно поэтому бетонную смесь следует производить теплой от +15 до + 25 °С.
- ПМД позволяют ускорить процесс гидратации цемента для достижения критической прочности. Важно, чтобы к моменту начала активного льдообразования цемент успел прореагировать с водой.
 А твердеющий цементный камень уже способен противостоять разрывающему усилию замерзающей воды, которая не поместилась в поры и капилляры. Исследованиями многих мировых ученых установлено, что бетоны с противоморозными добавками при достижении некой начальной «критической» прочности уже способны безболезненно выдерживать последующее замораживание.
А твердеющий цементный камень уже способен противостоять разрывающему усилию замерзающей воды, которая не поместилась в поры и капилляры. Исследованиями многих мировых ученых установлено, что бетоны с противоморозными добавками при достижении некой начальной «критической» прочности уже способны безболезненно выдерживать последующее замораживание.
Критическая прочность – прочность бетона на сжатие, при достижении которой, возможно последующее «безболезненное» замораживание бетона.
В соответствии с различными мировыми рекомендациями и в зависимости от класса бетона, критическая прочность бетона составляет в среднем от 10 МПа или 30% от требуемой прочности на 28 сут. нормального твердения.
- Растворы ПМД в виде солей представляют собой растворы электролитов, которые повышают электропроводимость бетона и способствуют повышению эффективности электропрогрева.
Необходимо обратить внимание на пластификаторы, которые оказывают влияние на твердение бетона зимой.
Вода снижает все показатели цементного камня, и в первую очередь, скорость схватывания, конечную прочность и эксплуатационную долговечность.
Если летом это практически незаметно, то при температурах ниже +10°С влияние «дополнительной» воды становится определяющим, а при +5°С и ниже — решающим в процессе схватывания цемента. Поэтому правильный подбор пластификатора и снижение водоцементного отношения поможет получить наилучший результат при зимнем бетонировании.
Подводя небольшой итог, можем сказать, что для зимнего бетонирования наиболее эффективным решением является комплексное использование связки «пластификатор-ускоритель».
В нашем портфолио продукты для зимнего бетонирования представлены в различных линейках MasterPozzolith, MasterRheobuild, MasterPolyheed, MasterGlenium:
Противоморозные добавки (ускорители) на основе солей электролитов:
- MasterPozzolith 501, MasterPozzolith 503, MasterPozzolith 506, MasterPozzolith 507, MasterPozzolith 515
Комплексные решения 2 в 1 c пластификаторами:
При какой температуре замерзает вода – самая полная информация!
Большинство людей уверены, что знают, при какой температуре замерзает вода – ниже 0 градусов по шкале Цельсия.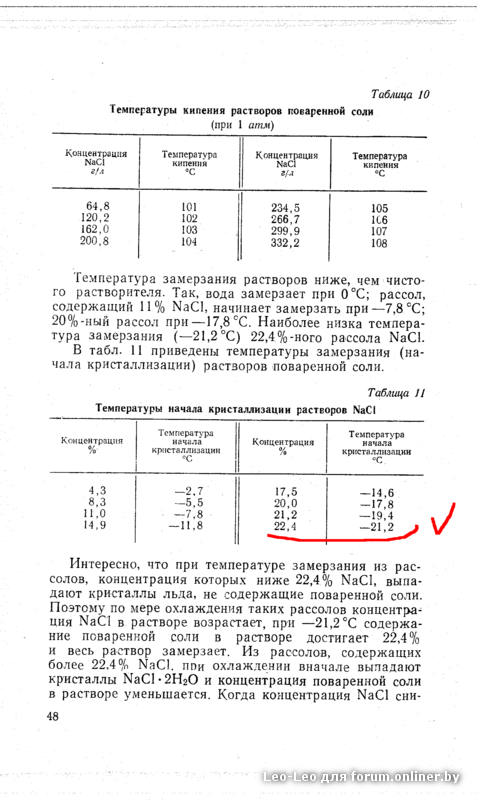 Однако так случается далеко не всегда. Не верите? Тогда читайте нашу статью – в ней мы подробно рассмотрим различные условия.
Однако так случается далеко не всегда. Не верите? Тогда читайте нашу статью – в ней мы подробно рассмотрим различные условия.
Пресные водоемы
В любых пресных водоемах, в том числе в реках, вода замерзает при температуре в 0 градусов. Например, самые чистые ручьи и небольшие речки промерзать начинают … с дна! Первоначально ледовый налет образовывается на корягах и прочих присутствующих в воде растениях и предметах. А когда этот ледовый налет поднимается наверх, река водоем сразу же замерзает.
Дистиллированная вода
Дистиллированная вода являет собой жидкость, прошедшую особую очистку. В ней нет никаких примесей, а также полностью отсутствуют так называемые ядра кристаллизации, которые и обеспечивают замерзание.
Поэтому образование льда в дистиллированной воде происходит при довольно низких температурах – лишь, когда столбик термометра опускается к отметке в -42 градуса.
Хотя исследователям удалось добиться такого уровня дистилляция, что полученная жидкость не замерзала до того момента, пока температура не достигла отметки в -70 градусов.
Кстати, такая жидкость, которая охлаждена до крайне низких температур, но так и не замерзла, получила название переохлажденной.
Замерзание соленой воды
Многие интересуются, при какой температуре замерзает морская вода, ведь в ней присутствует большое количество соли.
Итак, уровень температуры соленой воды, при которой она начнет замерзать, составляет не более -1,9 градусов.
Кстати, знаете ли вы, что используется специальная соль для очистки воды? Она засыпается в особые виды фильтров.
В результате исследований было установлено, что средняя температура замерзания морей планеты составляет -4 градуса по Цельсию. Однако этот показатель непостоянный – в разных морях он разный, что обусловлено не только уровнем содержания соли, но и прочими факторами:
- Каспий начинает замерзать, если температура опустится всего лишь на полградуса ниже нулевой отметки;
- Азовское море покрывается льдом, если температура воды опустится до отметки в -0,7 градуса.
 Лед сковывает воды Азова примерно с конца декабря и по начало марта. В некоторых местах толщина ледового покрытия достигает одного метра;
Лед сковывает воды Азова примерно с конца декабря и по начало марта. В некоторых местах толщина ледового покрытия достигает одного метра; - Японское море вообще не замерзает, что обусловлено повышенным содержанием соли – этот уровень равняется 34 промилле;
- Балтийское море имеет наименьшее содержание соли из всех вышеперечисленных морей и замерзает при охлаждении воды до 0 градусов.
Как видите, далеко не всегда вода замерзает при температуре в 0 градусов – возможны и исключения. Которые, кстати, не редкие!
А чтобы получать дома чистую и приятную воду дома, рекомендуем установить системы обратного осмоса.
основные способы и инструкции по приготовлению растворов с добавками
Несомненно, заниматься строительством в зимнее время сложнее, чем летом. Чаще всего погодные условия не слишком располагают к выполнению качественной работы. Обычно трудиться в суровые морозы продолжают либо профессиональные строительные бригады, либо же мастера, которые желают вселиться в собственное жилье как можно скорее. Неоценимой помощью для тех и других станут специализированные противоморозные добавки. Применение последних позволяет предотвратить преждевременное застывание цемента.
Неоценимой помощью для тех и других станут специализированные противоморозные добавки. Применение последних позволяет предотвратить преждевременное застывание цемента.
Что представляет собой противоморозная добавка в раствор?
Как правило, при значительном понижении температуры окружающей среды строители начинают испытывать дополнительные трудности в ходе работы с бетоном и всевозможными растворами. Все потому, что составы на основе цемента не выносят морозов. Так, при температуре в -5 оС, казалось бы, качественные растворы перестают набирать прочность.
В последние годы мастера все чаще применяют противоморозные добавки, способные выдержать понижение температуры до -35 оС и более. Специализированные составы для цементных растворов содержат химические вещества, действующие компоненты которых снижают температуру замерзания воды. В результате бетон схватывается в кладке даже в сильный холод.
Антиморозные добавки своими руками
В частном строительстве, если не удалось провести все работы в теплое время года, приходится продолжать в зимний период. Поэтому допускается приготовление противоморозных добавок для бетона своими руками в домашних условиях. Для этого понадобится только поваренная соль или хлорид натрия. Такая присадка снижает температуру замерзания воды и уменьшает время критичного затвердевания смеси.
Поэтому допускается приготовление противоморозных добавок для бетона своими руками в домашних условиях. Для этого понадобится только поваренная соль или хлорид натрия. Такая присадка снижает температуру замерзания воды и уменьшает время критичного затвердевания смеси.
Чтобы сделать противоморозную добавку в бетон своими руками, соль растворяется в воде и добавляется в раствор. Концентрация до -5 градусов составляет 2% от массы раствора, до -15 градусов, массовая доля хлорида достигает 4%.
Недостатком этой добавки является коррозионная активность по отношению к металлу, поэтому она не подходит для железобетонных конструкций. Нужно учитывать, что скорость затвердевания раствора при отрицательных температурах будет, в среднем, в 3 раза ниже, чем в обычных условиях.
Проблема организации кирпичной кладки в морозы
При ведении строительства в зимнее время становится наиболее проблематично обеспечить конструкциям необходимую прочность. Когда температура падает ниже нуля, жидкость в составе раствора кристаллизируется. Таким образом, прекращается процесс гидратации цемента.
Таким образом, прекращается процесс гидратации цемента.
При повышении температуры воздуха лед, образованный внутри кладки и на поверхности стройматериала, начинает подтаивать, что обязательно вызывает снижение сцепления раствора. Другим негативным эффектом становится образование мелких полостей в структуре бетона, что впоследствии может привести к довольно быстрому разрушению стен и перекрытий.
Если бетон замерз, не успев набрать необходимую прочность
О том, как ведет себя бетон при зимнем бетонировании подробно рассказано в статье о схватывание бетона при низких температурах. А что произойдет, если температура воздуха неожиданно опустится ниже нуля и бетон все-таки замерзнет?
В том случае, если понижение температуры – явление временное и в скором времени положительная температура восстанавливается, вода в бетоне оттаивает, процесс гидратации цемента (набора прочности) возобновляется. “Примороженный” ненадолго ранний бетон практически ничего не потеряет. Конечно, не обойдется без некоторого снижения заявленной марочной прочности, но оно будет не столь критично.
Обычно, в подмороженном бетоне портится только самый верхний слой. Так, к примеру, у отлитой фундаментной плиты от внезапных заморозков пострадает только поверхность, которая со временем облупится, подобно шелухе. Тому есть причины:
Первая: внутреннюю часть бетонной конструкции спасет тепло, которое выделяется при изотермической химической реакции цемента с водой. Плюс защитная функция опалубки и внешнего слоя бетонной конструкции.
Вторая: вода, будучи самым легким компонентом бетона, всегда поднимается наверх. В результате в верхней части плиты некоторая часть воды получается лишней, то есть водоцементное соотношение нарушено. Прибавим мороз и – отсюда – ломкий верхний слой
Гораздо плачевнее ситуация, когда мороз ударил надолго, оттепелей не ожидается, и бетону нет никакой возможности “оттаять” и “добрать” необходимую прочность. В этом случае нужно попытаться хоть как-то спасти ситуацию: закрыть бетонную конструкцию утеплителями или плёнкой ПВХ, чтобы оттепели и заморозки, неизменно происходящие весной, нанесли минимум вреда и без того слабому верхнему слою бетона. После этих мер, у цемента будет хоть какой-то шанс продолжить весной процесс гидратации. Очевидно, что прочность будет ниже, чем у расчётной марки бетона, но еще хуже оставить неокрепший бетон просто брошенным под дождем и снегом.
После этих мер, у цемента будет хоть какой-то шанс продолжить весной процесс гидратации. Очевидно, что прочность будет ниже, чем у расчётной марки бетона, но еще хуже оставить неокрепший бетон просто брошенным под дождем и снегом.
Несомненно, мусорные пакеты одно из самых ценных изобретений современности: удобно, дешево, надежно и практично. Пакеты для мусора различаются по объемам и прочности, материалам и технологии изготовления, удовлетворяя любым нуждам и потребностям населения.
Особенности подготовки раствора
Несмотря на сложные условия работы, кладка кирпича зимой может быть не менее качественной, чем в теплый период года. Однако чтобы получить ожидаемый результат, необходимо подготовить особый раствор, в составе которого обязательно должны присутствовать противоморозные добавки.
Приступая к приготовлению строительной смеси, необходимо позаботиться о личной безопасности. Следует учитывать, что практически все противоморозные добавки отличаются составом на основе достаточно агрессивных химических веществ, которые могут причинить вред здоровью. Поэтому в ходе подготовки бетона работать нужно в плотных перчатках, защитных очках, резиновых сапогах и по возможности в спецодежде.
Поэтому в ходе подготовки бетона работать нужно в плотных перчатках, защитных очках, резиновых сапогах и по возможности в спецодежде.
По вышеуказанной причине строительные смеси с содержанием ядовитых веществ не рекомендуется использовать при возведении фундаментов и несущих стен строений. Также противоморозные добавки в раствор для кладки запрещено применять для выполнения работ внутри жилых помещений.
Как рассчитать дозировку?
Доза компонента, применяемого в качестве добавки, препятствующего замерзанию бетона или раствора зимой, определяется строго по инструкции, имеющейся на упаковке.
Следует учитывать что:
- Реагент никогда не добавляется в сухую смесь.
- Для некоторых ядовитых добавок (например, для нитрида натрия) существует предельно допустимая концентрация (для НН – это не более 5 мг/л).
- Дозировка всегда исходит от объема приготовляемой бетонной или растворной смеси (опять же, следует внимательно читать инструкцию).

Виды противоморозных добавок
Чтобы цементный шов успел приобрести достаточный уровень прочности до момента замерзания жидкости, специалисты традиционно используют следующие противоморозные добавки в раствор для кладки:
- Поташ (углекислый калий).
- Формиат натрия.
- Хлористый натрий.
- Нитрит натрия (азотистый натрий).
- Хлористый калий.
Для проведения работ в условиях понижения температуры окружающей среды до -15 оС оптимальным решением станет применение противоморозных добавок в виде нитрита и формиата натрия.
При более серьезном похолодании до -30 оС целесообразно использовать поташ. Преимущество данного решения – защита от проявлений коррозии в случае возведения армированных перекрытий. Применение поташа также позволяет предотвратить появление высолов на затвердевшем растворе. Что касается хлорсодержащих добавок, последние не замедляют разрушение армирующих деталей строительных конструкций.
Мифы, связанные с добавками
График прогрева бетонного монолита.
- В широком использовании данный вид присадок появился не так давно. Народ еще не успел, как следует разобраться в том насколько это удобно и на этой благодатной почве родилось несколько предубеждений.
- Первый распространенный миф родился уже давно, периодически с появлением каждого нового состава подымается данный вопрос, не стали исключением и морозоустойчивые добавки. Кустарные мастера «авторитетно» заявляют о том, что такие добавки вызывают повышенную коррозию арматурного каркаса.
- Возьмем самый простой и доступный в России нитрит натрия. Любой средний химик или специалист по металловеденью вам скажет, что это один из ингибиторов способных замедлять процессы коррозии. Более того, в соединении с пластификаторами и усадочными добавками для работы с монолитами, в виду повышения крепости может применяться только алмазное бурение отверстий в бетоне, а также резка железобетона алмазными кругами.
Соотношение компонентов в разных марках чистого бетона.
- Вторым распространенным мифом можно назвать снижение прочности бетона. Родилось это утверждение из-за того, что на первых этапах схватывания раствора действительно наблюдается некоторое запоздание по сравнению с чистым бетоном. Но зато впоследствии скорость набора прочности значительно увеличивается. Особенно это относится к комбинированным составам.
- Все специалисты, с самого начала советуют одно, внимательно изучить инструкцию. При недостаточном количестве присадки в растворе, он может замерзнуть. Но если заложить чрезмерно много добавки, то вы рискуете увеличить время схватывания или потерять определенный процент крепости из-за образования газов.
На видео в этой статье вы можете открыть для себя много полезных мелочей.
Противоморозная добавка: расход
При изготовлении составов для кирпичной кладки важно соблюдать необходимые пропорции. Зависят они, в первую очередь, от температуры окружающей среды.
Давайте рассмотрим усредненные нормы, характерные для применения наиболее востребованных «антифризов», в таблице. Она отражает расход противоморозных добавок в процентном соотношении к массе цемента.
Она отражает расход противоморозных добавок в процентном соотношении к массе цемента.
| Температура воздуха | Формиат натрия | Поташ | Нитрит натрия |
| -5 оС | 2-3 % | 5-6 % | 4-6 % |
| -10 оС | 3-4 % | 6-8 % | 6-8 % |
| -15 оС | 4-5 % | 8-10 % | 8-10 % |
Пластификаторы
Противоморозная добавка в раствор может заменяться специальными пластификаторами, которые повышают эластичность строительной смеси и снижают необходимость в применении жидкости. Благодаря использованию последних на протяжении нескольких суток в уложенном составе практически не происходит изменений. Таким образом, раствор успевает схватиться даже при существенных морозах.
Помимо кладки, применяться может такая специфическая противоморозная добавка для клея, подготовки смесей для обустройства наливных полов, при выполнении бетонных работ. Пластифицирующие вещества смешиваются с минимальным количеством воды.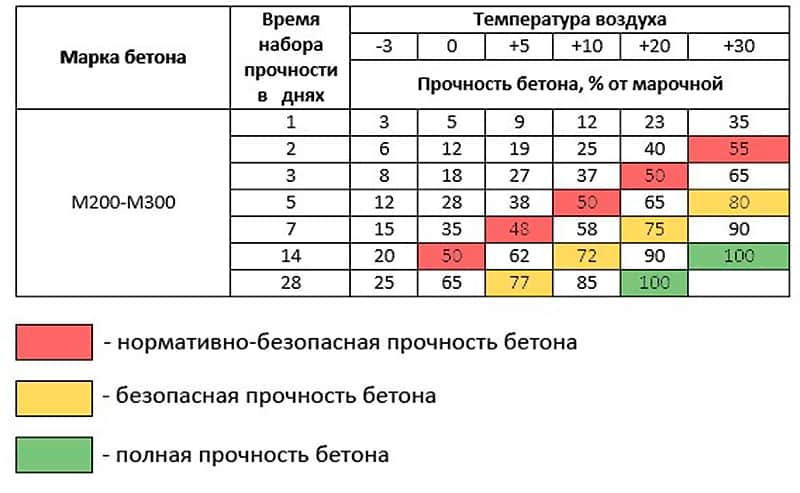 Их содержание в растворе составляет порядка 5 % от веса цемента. Соблюдения данной пропорции достаточно для выполнения надежной кладки в условиях пониженных температур.
Их содержание в растворе составляет порядка 5 % от веса цемента. Соблюдения данной пропорции достаточно для выполнения надежной кладки в условиях пониженных температур.
Бетонирование при низких температурах
Бетонирование при низких температурах связано с определенными сложностями. Основной задачей при бетонировании в условиях низкой температуры является предотвращение замерзания воды в растворе бетона, что может привести, как к засыханию, так и к замерзанию бетонного раствора.
Чтобы предотвратить замерзание бетонного раствора на современных стройках, создают все необходимые для этого условия:
• Бетон укрывают ПВХ пленками, либо используют разнообразные утеплители. Это самый доступный метод для того, чтобы бетонный раствор не замерз, но эффект от него можно получить только в том случае, если температура воздуха составляет от +5 до -5 градусов. Если же температура ниже -5 градусов, то применение утеплителей и пленки не целесообразно.
• Применяют электрическое прогревание раствора бетона. Такой метод предотвращения замерзания бетонного раствора, часто применяется на очень крупных объектах строительства, где имеются трансформаторные подстанции, которые могут обеспечить бесперебойное поступление электроэнергии. Это очень дорогой способ защиты бетонного раствора от замерзания, и его применение необходимо только в том случае, если застройщик не усевает сдать объект в установленный срок. На мелких объектах строительства применение данного способа не целесообразно.
Такой метод предотвращения замерзания бетонного раствора, часто применяется на очень крупных объектах строительства, где имеются трансформаторные подстанции, которые могут обеспечить бесперебойное поступление электроэнергии. Это очень дорогой способ защиты бетонного раствора от замерзания, и его применение необходимо только в том случае, если застройщик не усевает сдать объект в установленный срок. На мелких объектах строительства применение данного способа не целесообразно.
• В бетонный раствор добавляют специальную противоморозную добавку, которая предотвращает преждевременное замерзание раствора. Во многих случаях данная добавка уже входит в состав цемента, который представляет собой основной ингредиент любой марки бетонной смеси. Количественный процент соотношения цемента и добавок зависит от температуры, при которой будет непосредственно проводиться процесс бетонирования. Более точную информацию о том, какую добавку и в каком количестве лучше всего использовать, обязан предоставить производитель бетонной смеси в технической карте изделия.
• Возводят так называемые времянки, которые нужны для прогревания бетонных растворов непосредственно при помощи тепловыделяющего оборудования. Здесь необходимо обязательное использование ПВХ пленки и разнообразного рода утеплителей, но это нужно не для того, чтобы накрыть бетонный раствор, а непосредственно для утепления самого помещения времянки.
Производя бетонные работы при низких температурах, нужно помнить об обязательном соблюдении условий для затвердения бетонной смеси в течение всего срока, необходимого для достижения бетонной смесью минимальной прочности. Использование бетонного раствора при низких температурах подразумевает обязательное использование специальных добавок, которые способствуют ускорению процесса затвердения бетонного покрытия. Вследствие воздействия низких температур во время застывания значительно страдает качество бетона, идет частичное разрушение верхнего покрова, а также появляется коррозия на используемой арматуре, что непосредственно снижает качество производимых работ.
Низкая температура оказывает негативное влияние на бетон свежей укладки. Это хорошо ощущается в момент схватывания и затвердения смеси. Отсюда можно сделать вывод, что низкая температура воздуха способствует медленному застыванию бетонного раствора, что плохо влияет на качество выполненных работ. При минусовой температуре вода, используемая в приготовлении бетонного раствора, замерзает, что непосредственно прекращает процесс твердения бетонного раствора. Замерзшая вода приводит к разрушению верхнего бетонного покрытия, что негативно сказывается на его качестве и полноценном вводе в эксплуатацию. После того, как раствор нагреется — вода оттает, и в бетоне возобновятся все необходимые процессы. Но тогда свойства бетонного раствора будут иметь отличия от начального состава, что непосредственно скажется на таких факторах как: долговечность, прочность, водонепроницаемость и так далее.
Что нужно знать о выполнении кладочных работ в зимнее время?
Чтобы не разочароваться в результатах строительных мероприятий, которые выполняются при отрицательных показателях температуры воздуха, достаточно обратить внимание на следующие рекомендации:
- Для кладки запрещено использовать стройматериалы, покрытые снегом, инеем или наледью.

- Все компоненты будущего раствора, включая противоморозные добавки и пластификаторы, должны храниться в сухих, проветриваемых помещениях при комнатной температуре.
- Независимо от состава раствора и температурных условий кладку в зимнее время рекомендуется выполнять как можно быстрее. Отсутствие промедлений позволяет веществам схватиться быстрее.
- Отправляясь на перерыв, ряды кладки необходимо утеплить полиэтиленовой пленкой либо другим походящим материалом, подходящим на роль эффективного временного изолятора.
- В качестве основы для приготовления раствора стоит использовать цемент марки не ниже М-50. Смешивание компонентов даже в случае применения «антифризов» следует проводить в теплом помещении.
- При необходимости работы при пониженных температурах предпочтение лучше отдавать приобретению готовых растворов, в которые добавляются противоморозные вещества в оптимальных пропорциях еще на стадии производства.
Принцип действия и виды морозостойких составов
Загрузка в бетономешалку.
Что добавлять в бетон при минусовой температуре, вопрос далеко не праздный. Полностью, на 100% универсального состава не существует.
Выбор зависит от многих факторов, прежде всего от самой температуры.
- Также большое влияние оказывает размер монолита. Плюс следует учесть предназначение изделия, дело в том, что разные добавки могут менять некоторые физические качества бетона и то, что подойдет для ленточного фундамента в частном доме, может не подойти для возведения моста или крупного наливного цоколя.
Прогрев методом «Термос».
Как это работает
Как известно основной задачей воды в растворе является создание условий для кристаллизации составляющих раствора, силикатов, алюминатов и так далее. На языке профессионалов это называется гидратацией цемента.
Наиболее комфортно, без добавок, раствор застывает при температуре 15 — 20 ºС, все что выше и особенно ниже, нуждается в создании специальных условий.
- Главной задачей подобного рода присадок является снижение периода схватывания раствора и уменьшение времени созревания бетона при низких температурах.
 То есть снизить уровень замерзания воды и при этом не навредить остальным процессам, происходящим в растворе.
То есть снизить уровень замерзания воды и при этом не навредить остальным процессам, происходящим в растворе.
Зависимость набора прочности от температуры.
Распространенные составы и способы работы
- Наиболее распространенными материалами для изготовления морозоустойчивых присадок смело можно считать соли монокарбоновых кислот, среди профессионалов этот состав известен как «Поташ». Цена на данные составы на отечественном рынке вполне приемлемая.
- Когда выполняется заливка бетона при минусовой температуре добавки монокарбоновых кислот, должны строго дозироваться. Для каждой температуры количество присадок разное, Такими добавками можно подготовить раствор к температуре до минус 30ºС. Чем ниже температура, тем больше состава потребуется.
Соль монокарбоновой кислоты.
Важно: как говорилось ранее, присадка при неграмотном использовании может понизить другие характеристики раствора. Поэтому принцип, чем больше, тем лучше здесь может навредить.
- Следующим лидером нашего рынка является нитрит натрия. Цена на него также не сильно высока, но это вещество обладает сильным, едким, неприятным запахом. Кроме того данный состав легко может воспламениться. При контакте с некоторыми видами современных пластификаторов могут выделяться ядовитые, токсичные газы.
Нитрит натрия.
- Максимальная температура, которую может держать нитрат натрия, составляет не ниже -15ºС. Специалисты рекомендуют его использование при приготовлении растворов на портландцементе или на шлакопортландцементе. Добавлять эту присадку в глиноземистые цементы строго запрещено.
- Широкий спектр использования имеет формиат натрия и нитрат кальция. Кроме производства ЖБИ, эти присадки могут применяться в штукатурных растворах и растворах предназначенных для кладки кирпича. Но данные составы используются только в комплексе с пластификатором, так как из-за скопления солей, в монолите могут образовываться пустоты и высолы.

Формиат натрия.
Важно: растворы с добавлением присадок должны готовиться своими руками при температуре не ниже 5 — 10 ºС. Кроме того, они не могут долго храниться, раствор нужно использовать в течение часа после замешивания.
Строительный тепловентилятор.
- Не стоит забывать об отечественных производителях, добавки из линейки морозо-пласт, морозо-стирол и т.д. Являются составами комплексного действия, после заливки благодаря процессам, происходящим внутри монолита, температура поддерживается естественным образом и при небольших морозах, вам достаточно просто хорошо укрыть бетон.
Зависимость от марки бетона
Конструкции для электроподогрева монолита.
- По нормам СНиП 111-1-76, мороз опасен для бетона только на стадии набора прочности. Поддерживать определенную температуру в монолите нужно до определенного % крепости. Для каждой марки бетона этот процент индивидуален.
- После того, как монолит схватился, замораживание ему уже не настолько страшно, но и эксплуатировать ЖБИ еще не рекомендуется.
 Дело в том, что после оттаивания, изделие естественным путем будет дозревать. Активная фаза застывания монолита идет в течение 27 суток. После этого укрепление будет продолжаться еще несколько лет, но гораздо медленнее.
Дело в том, что после оттаивания, изделие естественным путем будет дозревать. Активная фаза застывания монолита идет в течение 27 суток. После этого укрепление будет продолжаться еще несколько лет, но гораздо медленнее. - Если в состав не вводились морозоустойчивые присадки, то для растворов с маркой М150 достаточно 50% прочности. Марки М200 – М300, могут замораживаться при 40% прочности. Для М400 и более, достаточно 30%. Но при использовании присадки, допустимая прочность перед замораживанием падает в среднем на 10%.
Совет: время вымешивания состава в зимних условиях должно быть увеличено минимум в 2 раза.
В итоге
При выполнении строительных работ в зимнее время главное — не забывать добавлять в раствор специальные противоморозные добавки. Впрочем, введение «антифризов» в цементный состав выглядит целесообразным лишь в случае понижения температуры окружающей среды до -5 оС.
В ходе подготовки раствора абсолютно не рекомендуется использовать давно хранившиеся, старые противоморозные добавки с сомнительным сроком годности. В противном случае придется расплачиваться образованием обильных подтеков и высолов на поверхности конструкций.
В противном случае придется расплачиваться образованием обильных подтеков и высолов на поверхности конструкций.
Бетонирование зимой
Проводить бетонные работы в зимнее время (например возводить стены по методу бетонной опалубки или заливать монолитное перекрытие) специалисты рекомендуют при температуре воздуха не ниже -10 «С. При более сильных морозах бетонирование лучше временно прекратить. «Свежую» конструкцию надо накрыть рубероидом, полиэтиленовой пленкой или минеральной ватой на несколько дней, пока бетон надежно не схватится.
Бетономешалка подойдет, если рабочих много или готовый раствор можно хранить в отапливаемом помещении
Раствор, оставленный на открытом воздухе, рискует быстро замерзнуть и прийти в негодность
В противном случае смесь стоит готовить небольшими порциями
Зачем мы зимой посыпаем солью обледеневшие тротуары?
[ Примечание редактора: в своем ответе на этот вопрос покойный Джон Маргрейв утверждал, что соль растворяется в воде в виде ионов натрия и хлора, и эти ионы гидратируют или присоединяются к молекулам воды. В ходе этого процесса выделяется тепло, которое оттаивает лед. Ряд читателей предупредил нас о проблемах с этим объяснением. Профессор химического машиностроения Артур Пелтон из Университета Монреаля внес репрезентативную поправку. Далее следует его объяснение, а ниже приводится первоначальный ответ Маркгрейва. ]
В ходе этого процесса выделяется тепло, которое оттаивает лед. Ряд читателей предупредил нас о проблемах с этим объяснением. Профессор химического машиностроения Артур Пелтон из Университета Монреаля внес репрезентативную поправку. Далее следует его объяснение, а ниже приводится первоначальный ответ Маркгрейва. ]
Хотя в процессе гидратации выделяется тепло, оно с лихвой компенсируется теплом, поглощаемым при начальном разложении соли на ионы. Другими словами, весь процесс растворения — разложение на ионы плюс гидратация — поглощает тепло. Это легко продемонстрировать: налейте немного воды в стакан и проверьте ее температуру пальцем. Добавьте немного соли, перемешайте и снова проверьте. Температура снизится.
Фактическая причина того, что применение соли вызывает таяние льда, заключается в том, что раствор воды и растворенной соли имеет более низкую температуру замерзания, чем чистая вода.При добавлении ко льду соль сначала растворяется в пленке жидкой воды, всегда присутствующей на поверхности, тем самым понижая температуру ее замерзания ниже температуры льда. Поэтому лед при контакте с соленой водой тает, создавая более жидкую воду, которая растворяет больше соли, тем самым вызывая таяние большего количества льда, и так далее. Чем выше концентрация растворенной соли, тем ниже ее общая температура замерзания. Однако существует ограничение на количество соли, которое можно растворить в воде. Вода, содержащая максимальное количество растворенной соли, имеет температуру замерзания около нуля градусов по Фаренгейту.Следовательно, применение соли не растопит лед на тротуаре, если температура ниже нуля градусов по Фаренгейту.
Поэтому лед при контакте с соленой водой тает, создавая более жидкую воду, которая растворяет больше соли, тем самым вызывая таяние большего количества льда, и так далее. Чем выше концентрация растворенной соли, тем ниже ее общая температура замерзания. Однако существует ограничение на количество соли, которое можно растворить в воде. Вода, содержащая максимальное количество растворенной соли, имеет температуру замерзания около нуля градусов по Фаренгейту.Следовательно, применение соли не растопит лед на тротуаре, если температура ниже нуля градусов по Фаренгейту.
Чтобы понять, почему вода, содержащая растворенные соли, имеет более низкую температуру замерзания, чем чистая вода, учтите, что при контакте льда и воды происходит динамический обмен на границе двух фазовых состояний. Из-за тепловых колебаний во льду большое количество молекул в секунду отрывается от его поверхности и попадает в воду. За это же время большое количество молекул воды прикрепляется к поверхности льда и становится частью твердой фазы. При более высоких температурах первая скорость выше, чем вторая, и лед тает. При более низких температурах происходит обратное. В точке замерзания обе скорости равны. Если соль растворена в воде, скорость отрыва молекул льда не изменяется, но скорость, с которой молекулы воды прикрепляются к поверхности льда, уменьшается, главным образом потому, что концентрация молекул воды в жидкости (молекул на кубический сантиметр) ниже. Следовательно, температура плавления ниже.
При более высоких температурах первая скорость выше, чем вторая, и лед тает. При более низких температурах происходит обратное. В точке замерзания обе скорости равны. Если соль растворена в воде, скорость отрыва молекул льда не изменяется, но скорость, с которой молекулы воды прикрепляются к поверхности льда, уменьшается, главным образом потому, что концентрация молекул воды в жидкости (молекул на кубический сантиметр) ниже. Следовательно, температура плавления ниже.
Объясняет Джон Маргрейв, профессор химии Университета Райса.
Все ледяные поверхности содержат небольшие лужи воды. Поскольку соль растворима в воде, соль, нанесенная на такие поверхности, растворяется. Жидкая вода обладает так называемой высокой диэлектрической проницаемостью, которая позволяет ионам соли (положительно заряженному натрию и отрицательно заряженному хлору) разделяться. Эти ионы, в свою очередь, реагируют с молекулами воды и гидратируются, т. е. образуют гидратированные ионы (заряженные ионы, присоединенные к молекулам воды). В этом процессе выделяется тепло, поскольку гидраты более стабильны, чем отдельные ионы.Затем эта энергия плавит микроскопические части поверхности льда. Таким образом, значительное количество соли, разбросанной по большой поверхности, может фактически растопить лед. Кроме того, если вы едете по льду в своем автомобиле, давление помогает вдавливать соль в лед, и происходит дополнительное увлажнение.
В этом процессе выделяется тепло, поскольку гидраты более стабильны, чем отдельные ионы.Затем эта энергия плавит микроскопические части поверхности льда. Таким образом, значительное количество соли, разбросанной по большой поверхности, может фактически растопить лед. Кроме того, если вы едете по льду в своем автомобиле, давление помогает вдавливать соль в лед, и происходит дополнительное увлажнение.
Каменная соль, применяемая зимой на обледенелых дорогах, — это то же самое вещество, которое выходит из вашей солонки. Единственная разница заключается в размере. Каменная соль представляет собой материал, который кристаллизовался в более крупные куски, тогда как поваренная соль была измельчена и измельчена до более или менее равномерного распределения по размеру.Хлористый кальций так же широко используется для растапливания льда на улицах, как и хлористый натрий. На самом деле, это дешевле, чем хлорид натрия. Компании производят большое количество хлорида кальция из рассолов и других природных материалов, которые можно использовать для той же цели.
Первоначально опубликовано 8 декабря 2003 г.
Мы все кричим о мороженом
Обзор
Вода замерзает при температуре 32°F (0°C). Добавление соли в воду снижает температуру замерзания. То, насколько низко опустится точка замерзания, зависит от количества соли в воде.Студенты будут делать домашнее мороженое, но «время замерзания» будет варьироваться с использованием разного количества соли, чтобы снизить температуру замерзания воды.
| ОБЩЕЕ ВРЕМЯ | 30 минут. |
|---|---|
| ПРИНАДЛЕЖНОСТИ | Для каждой пары учащихся: Один пластиковый пакет с застежкой-молнией для сэндвичей и один для заморозки; 4 унции молока, сливок или пополам; щепотка ванильного экстракта или 1 чайная ложка шоколадного сиропа; 2 чайные ложки сахара; 2 пластмассовые ложки Для занятий в классе: Несколько пакетов со льдом; Каменная соль |
| ПЕЧАТЬ/AV МАТЕРИАЛ | Нет |
| УЧИТЕЛЬ ПОДГОТОВКА | Нет |
| ФОКУС БЕЗОПАСНОСТИ | Защита от холода |
Процедура
- Для каждой пары учащихся смешайте молоко, сахар и ванильный/шоколадный сироп в пакете размером с бутерброд и закройте его.

- Предложите учащимся встряхивать/мять пакеты в течение одной минуты, чтобы тщательно перемешать содержимое.
- Поместите пакет в большой пластиковый пакет с застежкой-молнией для морозильной камеры и заполните его наполовину дробленым льдом.
- С шагом в 2 унции, до 10 унций, помещайте различное количество каменной соли в каждый большой пакет. Включите пару или двух студентов без добавления соли.
- Пусть каждая пара оценит, сколько времени потребуется, чтобы их смесь замерзла.
- Все учащиеся начинают одновременно, пусть они смешивают и взбивают пакетики в быстром темпе, пока содержимое не затвердеет.
- Запишите их время.
- Когда закончите, выбросьте большую сумку и съешьте мороженое.
Обсуждение
Пакеты с наибольшим количеством соли должны «заморозиться» первыми, а пакеты с меньшим количеством соли требуют больше времени. Чем выше содержание соли, тем ниже температура замерзания воды, и, следовательно, более холодный раствор соленой воды и льда быстрее приводит к образованию мороженого.
| Водоем | Точка замерзания |
|---|---|
| Балтийское море | 31,3°F (-0,3°C) |
| Черное море | 30,2°F (-1,0°C) |
| Океаны | 28,5°F (-2,0°C) |
| Красное море | 27,9°F (-2,6°C) |
| Большое Соленое озеро | 11,8°F (-11.2°С) |
| Мертвое море | -6,0°F (-21,1°C) |
Распространенное заблуждение, что соль заставляет лед таять быстрее. Соль не имеет ничего общего с тем, как быстро тает лед — она просто определяет, при какой температуре он будет таять (или замерзать). В таблице (справа) указаны средние температуры замерзания воды для различных водоемов в зависимости от их солености.
Самая низкая температура замерзания солевого раствора -6.0°F (-21,1°C). При этой температуре соль начинает кристаллизоваться из раствора вместе со льдом, пока раствор полностью не замерзнет. Ниже -6,0 ° F (-21,1 ° C) замороженный раствор представляет собой смесь отдельных кристаллов морской воды и кристаллов пресной воды, а не однородную смесь кристаллов морской воды.
При этой температуре соль начинает кристаллизоваться из раствора вместе со льдом, пока раствор полностью не замерзнет. Ниже -6,0 ° F (-21,1 ° C) замороженный раствор представляет собой смесь отдельных кристаллов морской воды и кристаллов пресной воды, а не однородную смесь кристаллов морской воды.
Мешочки без соли не замерзнут. Почти все, что растворяется в воде (или молоке), снижает температуру замерзания; например сахар. Соль используется на дорогах, потому что она недорогая.Добавление сахара в молоко понизило температуру замерзания ниже, чем у обычного льда (32 ° F), и поэтому оно не замерзнет.
Создание нации, готовой к погодным условиям
Воздействие холода может вызвать обморожение или переохлаждение и стать опасным для жизни. То, что представляет собой экстремальный холод, различается в разных частях страны. На Глубоком Юге температура, близкая к нулю, может считаться экстремальным холодом.
Низкие температуры могут нанести серьезный ущерб цитрусовым и другой растительности. Трубы могут замерзнуть и лопнуть в домах с плохой изоляцией или без отопления. На севере экстремальные холода означают температуры значительно ниже нуля.
Трубы могут замерзнуть и лопнуть в домах с плохой изоляцией или без отопления. На севере экстремальные холода означают температуры значительно ниже нуля.
Обморожение — это повреждение тканей тела, вызванное сильным холодом. Обморожение вызывает потерю чувствительности и побеление или бледность конечностей, таких как пальцы рук и ног, мочки ушей или кончик носа.
При обнаружении симптомов немедленно обратитесь за медицинской помощью! Если вам необходимо дождаться помощи, медленно согрейте пораженные участки. Однако, если у человека также проявляются признаки гипотермии, сначала согрейте центр тела, а затем конечности.
Почему мы зимой посыпаем дороги солью?
Каждую зиму в Шарлотте выпадает в среднем около 4 дюймов снега в год, но мы также получаем больше всего льда в год.
Что происходит, когда погода Шарлотты требует гололеда, снега и скользких дорог? Ну, это солевой раствор!
В преддверии зимы Департамент транспорта Шарлотты распылит влажную смесь из двух видов соли — хлорида натрия и хлорида магния — вместе с водой, чтобы сделать «соляной раствор» на ключевых улицах. Этот метод называется защитой от обледенения или предварительным увлажнением и используется во многих городах США в качестве превентивной меры до наступления ненастной погоды.
Этот метод называется защитой от обледенения или предварительным увлажнением и используется во многих городах США в качестве превентивной меры до наступления ненастной погоды.
После накопления осадков вы также можете увидеть грузовики с солью, разбрасывающие твердую каменную соль по заснеженным и обледенелым дорогам.
Так зачем они это делают? Почему соль растапливает лед и снег?
Соль вызывает явление, называемое снижением температуры замерзания, что означает понижение температуры замерзания воды.Вода обычно замерзает при 32 градусах по Фаренгейту, но когда вы добавляете соль, этот порог может упасть до 20 градусов по Фаренгейту. Это означает, что если снежная буря в этом районе имеет наружную температуру 30 градусов по Фаренгейту, поверхности, обработанные раствором соли, замерзнут только в том случае, если температура снаружи упадет еще на 10 градусов. Если посыпать солью лед, он растает по тем же причинам.
Когда лед растает в лужи соленой воды, он распространится на окружающие дороги, смешиваясь с другим близлежащим льдом. В конце концов, вся поверхность льда превратится в соляную жижу, которая не растает, пока температура снаружи не упадет значительно. Насколько быстро растает лед и насколько низкой станет температура замерзания этой лужи, будет зависеть от того, сколько соли вы добавите.
В конце концов, вся поверхность льда превратится в соляную жижу, которая не растает, пока температура снаружи не упадет значительно. Насколько быстро растает лед и насколько низкой станет температура замерзания этой лужи, будет зависеть от того, сколько соли вы добавите.
Точно так же, как соль снижает температуру замерзания воды при низких температурах, она также повышает точку кипения при высоких температурах. Вы можете увидеть этот принцип в действии при приготовлении пасты.
С небольшой помощью науки вы теперь можете наслаждаться своими снежными днями с безопасно посоленными дорожками и паровой кастрюлей с макаронами!
Может ли вода оставаться жидкой при температуре ниже нуля градусов Цельсия?
Категория: Химия Опубликовано: 9 декабря 2013 г.
Температура замерзания воды падает ниже нуля градусов Цельсия при приложении давления.Изображение общественного достояния, источник: Кристофер С. Бэрд.
Да, вода может оставаться жидкой при температуре ниже нуля градусов Цельсия. Есть несколько способов, как это может произойти.
Есть несколько способов, как это может произойти.
Во-первых, фазовое состояние вещества (газообразное, жидкое или твердое) сильно зависит как от его температуры , так и от давления. Для большинства жидкостей приложение давления повышает температуру, при которой жидкость замерзает до твердого состояния. Твердое тело образуется, когда свободные извилистые молекулы жидкости перемещаются достаточно медленно и достаточно близко, чтобы образовать прочные связи, удерживающие их на месте.Когда мы оказываем давление на жидкость, мы заставляем молекулы сближаться. Поэтому они могут образовывать стабильные связи и становиться твердыми, даже если их температура выше, чем точка замерзания при стандартном давлении. Хотя вода уникальна. Молекулы воды распространяются, когда они связываются в твердую кристаллическую структуру. Это расширяющееся действие приводит к тому, что лед становится менее плотным, чем жидкая вода, в результате чего лед плавает. Это растекающееся действие молекул воды во время замерзания также означает, что приложение давления к воде снижает температуру замерзания. Если вы приложите достаточное давление (что затрудняет распространение молекул воды в твердую структуру), вы можете получить жидкую воду на несколько градусов ниже нуля градусов по Цельсию.
Если вы приложите достаточное давление (что затрудняет распространение молекул воды в твердую структуру), вы можете получить жидкую воду на несколько градусов ниже нуля градусов по Цельсию.
Даже если вы не применяете давление, вы все равно можете получить жидкую воду при минусовых температурах с помощью добавок. Такие добавки, как соль, могут мешать химическому связыванию, необходимому для образования твердого вещества, и поэтому они могут снизить температуру замерзания воды. Соль состоит из сильных ионов натрия и хлора. При растворении в воде молекулы воды имеют тенденцию прилипать к ионам соли, а не друг к другу, и поэтому они не так легко замерзают.Когда вы добавляете больше соли в воду, ее точка замерзания продолжает падать, пока вода не достигнет насыщения и больше не сможет удерживать соль. Если вы добавите достаточное количество соли, температура замерзания воды может снизиться до -21 градуса по Цельсию. Этот факт означает, что вода при -21 градусе Цельсия все еще может оставаться жидкой, если добавить достаточное количество соли. Вместо того, чтобы удерживать жидкую воду от замерзания, это мощное свойство соли также можно использовать для превращения льда обратно в воду. Посыпание солью обледенелых тротуаров снижает температуру замерзания льда ниже температуры окружающей среды, и лед тает.Но посыпать солью обледенелые дорожки не поможет, если температура окружающего воздуха ниже -21 градуса по Цельсию. Влияние соли на температуру замерзания воды также оказывает сильное влияние на земные океаны.
Вместо того, чтобы удерживать жидкую воду от замерзания, это мощное свойство соли также можно использовать для превращения льда обратно в воду. Посыпание солью обледенелых тротуаров снижает температуру замерзания льда ниже температуры окружающей среды, и лед тает.Но посыпать солью обледенелые дорожки не поможет, если температура окружающего воздуха ниже -21 градуса по Цельсию. Влияние соли на температуру замерзания воды также оказывает сильное влияние на земные океаны.
Даже если вы не применяете давление и ничего не добавляете в воду, вы все равно можете получить жидкую воду при температуре ниже нуля градусов по Цельсию. Чтобы вода превратилась в лед, ей нужно на что-то замерзнуть, чтобы начать процесс. Мы называем эти отправные точки «центрами зарождения».В большинстве случаев небольшое количество пыли, примесей или даже небольшая вибрация в воде создают центры зародышеобразования, на которых вода замерзает. Но если ваша вода очень чистая и очень спокойная, молекулам воды не на чем кристаллизоваться. В результате вы можете охлаждать очень чистую воду значительно ниже нуля градусов Цельсия, не замерзая. Вода в таком состоянии называется «переохлажденной». При нормальном давлении чистая вода может быть переохлаждена примерно до -40 градусов по Цельсию. Переохлажденную воду удерживает от замерзания только отсутствие центров зародышеобразования.Следовательно, как только образуются центры зародышеобразования (которые могут быть такими же простыми, как вибрация), переохлажденная вода быстро замерзает. Ледяной дождь является естественным примером переохлажденной жидкой воды. Как только ледяной дождь попадает на объект на поверхности земли, этот объект обеспечивает центры зарождения, и дождь замерзает, превращаясь в лед.
В результате вы можете охлаждать очень чистую воду значительно ниже нуля градусов Цельсия, не замерзая. Вода в таком состоянии называется «переохлажденной». При нормальном давлении чистая вода может быть переохлаждена примерно до -40 градусов по Цельсию. Переохлажденную воду удерживает от замерзания только отсутствие центров зародышеобразования.Следовательно, как только образуются центры зародышеобразования (которые могут быть такими же простыми, как вибрация), переохлажденная вода быстро замерзает. Ледяной дождь является естественным примером переохлажденной жидкой воды. Как только ледяной дождь попадает на объект на поверхности земли, этот объект обеспечивает центры зарождения, и дождь замерзает, превращаясь в лед.
Темы:
замерзание, точка замерзания, ледяной дождь, лед, фазовая диаграмма, давление, переохлаждение, температура, вода
Наука о мороженом — Депрессия точки замерзания
Почему кубик льда твердый как камень, а шарик итальянского мороженого почти жидкий? Даже «простое» эскимо не такое твердое, как кубик льда из чистой воды. Вместо этого вы можете легко откусить немного. Разве это не интересно?
Вместо этого вы можете легко откусить немного. Разве это не интересно?
Мы уже сделали довольно много мороженого, довольно сложное мороженое с заварным кремом, супер простое мороженое всего из двух ингредиентов или семифреддо в итальянском стиле. Во всех случаях мы считали само собой разумеющимся, что мороженое не получилось твердым. Частично это связано с введением воздуха. Мороженое было сделано воздушным за счет добавления взбитых сливок или благодаря постоянному перемешиванию мороженицы.Но просто подача воздуха не помогает. Замораживание чистых взбитых сливок все равно даст довольно твердую ледяную структуру.
Приходит важность сахара (или алкоголя) и явления, называемого депрессией точки замерзания!
Что такое депрессия точки замерзания?
Депрессия температуры замерзания говорит о том, что температура замерзания смеси двух компонентов ниже, чем у отдельных компонентов. Он включает растворитель (например, воду) и растворенное вещество, которое вы будете смешивать с растворителем.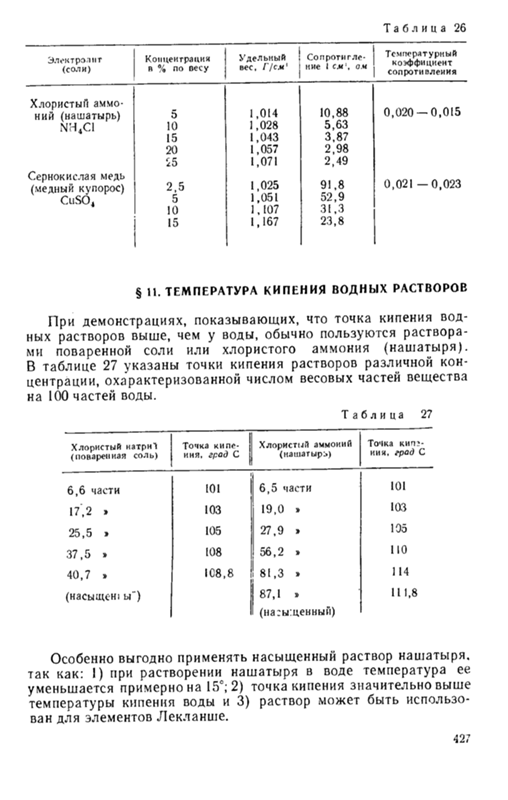
Очень частый пример такого явления в быту – засолка дорог водой. Чистая вода замерзает при 0°С. Однако при смешивании с солью температура замерзания этой смеси воды и соли упадет значительно ниже нуля. Вот почему соль используется для защиты дорог ото льда. Даже при отрицательных температурах на дороге не будет гололедицы.
Так почему же точка замерзания растворителя изменяется при растворении в нем чего-то другого? Что ж, если у вас есть только чистая вода (или любой другой растворитель), эти молекулы воды могут организоваться красиво и плотно.Когда температура понижается и вода замерзает, они могут образовать между собой красивый кристалл (подробнее о фазовых переходах). Однако при смешивании с растворенным веществом (например, солью или сахаром) эта хорошо упорядоченная структура нарушается. Вместо этого они могут образовывать эти кристаллы только при более низкой температуре. Это то, что происходит из-за депрессии точки замерзания.
Понижение точки замерзания мороженого
В мороженом изменена точка замерзания воды в мороженом. Вода является основным компонентом большинства мороженого, поскольку она составляет большую часть молока или сливок, которые вы можете использовать. Температура замерзания в основном снижается за счет добавления сахара. Сахар растворяется в воде и таким образом препятствует образованию кристаллов.
Вода является основным компонентом большинства мороженого, поскольку она составляет большую часть молока или сливок, которые вы можете использовать. Температура замерзания в основном снижается за счет добавления сахара. Сахар растворяется в воде и таким образом препятствует образованию кристаллов.
Вы также можете ожидать, что жир в мороженом повлияет на температуру замерзания. Однако это не так. Вода и масло не смешиваются, вместо этого маленькие пузырьки масла плавают в мороженом, но они никогда не мешают, как это делает сахар.
Алкоголь и мороженое
В различных рецептах для приготовления мороженого используется спирт. Помимо вкуса и алкоголя, он придает мороженому, он также используется для снижения температуры замерзания воды! Мороженое теоретически можно сделать без сахара и только с алкоголем, но не уверен, что получится так же вкусно…
Мороженое с большим количеством сахара
Расчет депрессии точки замерзания
Информационный бюллетень
Хотите быть в курсе новых статей о пищевых продуктах? Подпишитесь на нашу еженедельную рассылку
Вы можете легко рассчитать изменение точки замерзания воды в мороженом. Депрессия точки замерзания является так называемым коллигативным свойством. Это означает, что падение температуры, а значит, насколько снижается точка замерзания, не зависит от типа добавляемого компонента, растворенного вещества. Вместо этого это зависит только от количества добавленных частиц, а также от исходных свойств растворителя, к которому они добавляются.
Депрессия точки замерзания является так называемым коллигативным свойством. Это означает, что падение температуры, а значит, насколько снижается точка замерзания, не зависит от типа добавляемого компонента, растворенного вещества. Вместо этого это зависит только от количества добавленных частиц, а также от исходных свойств растворителя, к которому они добавляются.
Другими словами, если бы мы добавили 10 000 молекул сахара, это оказало бы такое же влияние на точку замерзания, как 10 000 частиц соли. Только когда количество растворенного вещества становится очень большим, становится важным тип растворенного вещества.
Из-за этой простой зависимости понижение точки замерзания можно рассчитать по простой формуле:
ΔT F = – K F · m · i
Где:
- ΔT F = изменение температуры замерзания в °C
- K F = криоскопическая постоянная, это значение зависит от используемого растворителя, для воды это 1853 °C·кг/моль
- m = моляльность растворенного вещества, другими словами, количество частиц на кг растворителя, в моль/кг растворитель, который вы должны принять во внимание, это наиболее характерно для солей.
 Для сахаров и т. п., которые не распадаются, эта константа равна единице, для хлорида натрия (соли) — две.
Для сахаров и т. п., которые не распадаются, эта константа равна единице, для хлорида натрия (соли) — две.
Расчет изменения температуры замерзания мороженого
Ванильное мороженое
Давайте посмотрим на изменение температуры замерзания обычного ванильного мороженого. Это мороженое содержит примерно 600 г (грубое предположение: 300 + 0,65 * 300 + 4 * 25) воды и 75 г сахара.
- Если сахар растворяется в воде, он не расщепляется, поэтому i в приведенной выше формуле равно 1, и мы также знаем значение криоскопической постоянной воды (1853 °C·кг/моль).
- Затем нам нужно узнать, сколько кристаллов сахара у нас есть. Из литературы мы установили, что 1 моль молекул сахара весит 342,3 г. Следовательно, 75 г сахара составляют 75/342,3 = 0,22 моль. Поскольку у нас есть 600 г воды, моляльность сахара составляет: 0,22 / 0,60 = 0,37 моль/кг.
Теперь нужно ввести формулу:
ΔT F = – K F · m · i = -1,853 · 0,37 · 1 = -0,68°C
Температура замерзания упала менее чем на 1 градус. На самом деле этого очень мало, поэтому это мороженое можно сделать намного мягче, добавив больше сахара.
На самом деле этого очень мало, поэтому это мороженое можно сделать намного мягче, добавив больше сахара.
Мягкое двухкомпонентное мороженое
Давайте сделаем еще один пример, чтобы попрактиковаться в этих вычислениях, теперь рассмотрим очень простое мороженое из двух ингредиентов. Это мороженое содержит 245 г воды (0,7 * 230 + 0,55 * 150) и 70 г сахара (0,45 * 150), для простоты мы округли числа.
Вы можете использовать многие из тех же чисел, что и в предыдущем расчете, но вам нужно рассчитать моляльность сахара для этого нового рецепта мороженого. Тем же методом находим: 70/342,3 = 0,20 моль и 0,02/0,245 = 0,83 моль/кг,
Заполним формулу еще раз:
ΔT F = -K F · m · i = -1,853 · 0,83 · 1 = -1,55°C
Фазовые диаграммы
Одно это изменение точки замерзания еще не говорит о полной истории мороженого, это только начало.Вместо этого, как только вы получите эти новые температуры, вы должны взглянуть на фазовую диаграмму. На фазовой диаграмме вы можете точно увидеть, сколько льда и жидкости будет присутствовать при разных температурах. Это слишком подробно для этого поста, но, к счастью, для вас есть отдельный пост на тему фазовых диаграмм.
На фазовой диаграмме вы можете точно увидеть, сколько льда и жидкости будет присутствовать при разных температурах. Это слишком подробно для этого поста, но, к счастью, для вас есть отдельный пост на тему фазовых диаграмм.
Примечание о замороженных фруктах
Вы когда-нибудь замечали, что замороженные фрукты часто бывают нетвердыми? Помимо влияния текстуры плода, это также связано с понижением температуры замерзания.Плоды содержат довольно много сахара, который не дает замерзнуть всей воде!
Видео для более подробного объяснения
Более фундаментальное объяснение можно найти в этом прекрасном видео от Академии Хана.
Ресурсы
Более подробное объяснение термодинамики понижения точки замерзания можно найти на веб-сайтах: UC Davis & Bristol University.
Уход за лошадью зимой
Нижняя критическая температура — это температура, ниже которой лошади требуется дополнительная энергия для поддержания тепла тела.Нижняя критическая температура для лошадей составляет 41°F в летней одежде и 18°F в зимней.
Факторы, влияющие на более низкую критическую температуру
Отдельные факторы, которые могут повлиять на более низкую критическую температуру лошади, включают длину шерсти и размер тела.
Лошадь с короткой шерстью, подвергающаяся воздействию холодной и влажной погоды, будет иметь более низкую критическую температуру, чем акклиматизированная к холоду лошадь с густой шерстью и запасами жира.
Мелкие животные имеют большую площадь поверхности по отношению к массе тела и могут терять тепло быстрее, чем более крупные животные.Отъемыши могут достичь своей более низкой критической температуры раньше взрослой лошади. Холодная погода может замедлить рост, потому что калории идут от набора веса на поддержание температуры. Чтобы уменьшить спад роста в холодную погоду, вы должны давать молодым лошадям дополнительные калории.
Чтобы уменьшить спад роста в холодную погоду, вы должны давать молодым лошадям дополнительные калории.
Более низкая критическая температура и потребность в энергии
Поскольку температура зимой снижается, лошади требуется дополнительная диетическая энергия для поддержания температуры и состояния тела. На каждый градус ниже 18 ° F лошади требуется дополнительный один процент энергии в их рационе.
Лучшим источником дополнительной пищевой энергии в холодные зимние месяцы являются корма.
Некоторые считают, что если давать больше зерна, лошади будет теплее. Но переваривание, всасывание и использование зерна не дает столько тепла, сколько микробная ферментация фуража. Больше корма увеличивает микробную ферментацию и согревает лошадь.
Если бездействующей лошади весом 1000 фунтов требуется 16 фунтов качественного сена ежедневно при температуре 18°F, ее потребность может увеличиться примерно в 2-2 раза. От 5 фунтов до 18-18,5 фунтов, если температура упадет до 0 ° F. Повышенная потребность в диетической энергии будет еще больше, если у лошади нет доступа к укрытию.
От 5 фунтов до 18-18,5 фунтов, если температура упадет до 0 ° F. Повышенная потребность в диетической энергии будет еще больше, если у лошади нет доступа к укрытию.
Почему морская вода не замерзает при нуле градусов?
Станьте свидетелем эксперимента, объясняющего, почему пресная и морская вода имеют разные точки замерзания
Узнайте, почему пресная и морская вода имеют разные точки замерзания.
Contunico © ZDF Enterprises GmbH, Майнц
Стенограмма
Вода — это то, что мы охотно используем, не задумываясь. Тем не менее, быть влажным не является характеристикой, присущей всем формам воды. Например, при нуле градусов по Цельсию вода начинает замерзать. В Университетском колледже Лондона химик Андреа Селлер проводит эксперимент, чтобы объяснить нам, почему соленая вода ведет себя иначе, чем пресная вода. Селлер начинает с миски с кубиками льда. Термометр показывает ноль градусов. Это и точка замерзания воды, и точка таяния льда. При нуле градусов вода и лед находятся в состоянии термодинамического равновесия. Молекулы воды высвобождаются изо льда, в то же время из воды образуются молекулы льда. Селлер добавляет в миску немного поваренной соли и перемешивает. Температура падает, но посмотрите на это, вода не замерзает. Причина этого связана с ионами хлорида натрия в растворе соленой воды, показанными здесь синими и красными кружками.Эти заряженные частицы нарушают баланс молекул, в результате чего количество молекул воды, которые могут зацепиться за молекулы льда, уменьшается. Таким образом, вода замерзает медленнее.
Термометр показывает ноль градусов. Это и точка замерзания воды, и точка таяния льда. При нуле градусов вода и лед находятся в состоянии термодинамического равновесия. Молекулы воды высвобождаются изо льда, в то же время из воды образуются молекулы льда. Селлер добавляет в миску немного поваренной соли и перемешивает. Температура падает, но посмотрите на это, вода не замерзает. Причина этого связана с ионами хлорида натрия в растворе соленой воды, показанными здесь синими и красными кружками.Эти заряженные частицы нарушают баланс молекул, в результате чего количество молекул воды, которые могут зацепиться за молекулы льда, уменьшается. Таким образом, вода замерзает медленнее.
Ученые называют эту практику понижением температуры замерзания. Химик итальянского происхождения добавляет в лед все больше и больше соли. Тем не менее, температура замерзания не может быть снижена до бесконечности и в конечном итоге стабилизируется на отметке 21 градус ниже нуля. Причина в том, что соль больше не может быть растворена в солевом растворе.

 Это явление называют депрессией точки замерзания.
Это явление называют депрессией точки замерзания. А твердеющий цементный камень уже способен противостоять разрывающему усилию замерзающей воды, которая не поместилась в поры и капилляры. Исследованиями многих мировых ученых установлено, что бетоны с противоморозными добавками при достижении некой начальной «критической» прочности уже способны безболезненно выдерживать последующее замораживание.
А твердеющий цементный камень уже способен противостоять разрывающему усилию замерзающей воды, которая не поместилась в поры и капилляры. Исследованиями многих мировых ученых установлено, что бетоны с противоморозными добавками при достижении некой начальной «критической» прочности уже способны безболезненно выдерживать последующее замораживание. Лед сковывает воды Азова примерно с конца декабря и по начало марта. В некоторых местах толщина ледового покрытия достигает одного метра;
Лед сковывает воды Азова примерно с конца декабря и по начало марта. В некоторых местах толщина ледового покрытия достигает одного метра;
 То есть снизить уровень замерзания воды и при этом не навредить остальным процессам, происходящим в растворе.
То есть снизить уровень замерзания воды и при этом не навредить остальным процессам, происходящим в растворе.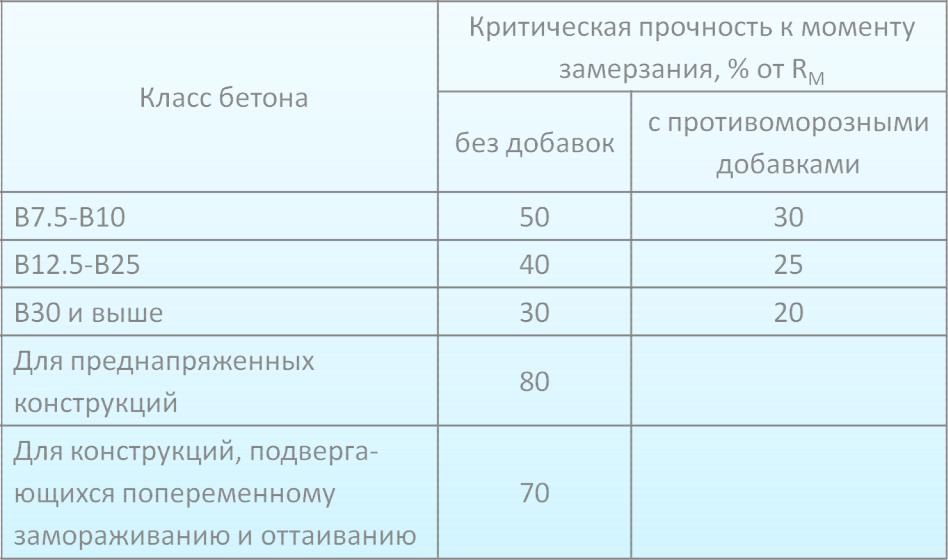
 Дело в том, что после оттаивания, изделие естественным путем будет дозревать. Активная фаза застывания монолита идет в течение 27 суток. После этого укрепление будет продолжаться еще несколько лет, но гораздо медленнее.
Дело в том, что после оттаивания, изделие естественным путем будет дозревать. Активная фаза застывания монолита идет в течение 27 суток. После этого укрепление будет продолжаться еще несколько лет, но гораздо медленнее.
 Для сахаров и т. п., которые не распадаются, эта константа равна единице, для хлорида натрия (соли) — две.
Для сахаров и т. п., которые не распадаются, эта константа равна единице, для хлорида натрия (соли) — две.